
Europska agencija za lijekove – izvješće o mastiki
- Objava objavljena:23. lipnja, 2023
- Vrijeme čitanja:78 min. čitanja
Na podlagi člena 16d(1), člena 16f in člena 16h Direktive 2001/83/ES (tradicionalna uporaba)
Rastlinska snov (binomsko znanstveno ime rastline, vključno z delom rastline) | Pistacia lentiscus L., resina (mastika) |
Zeliščni pripravek(-i) | Rastlinska snov v prahu |
Farmacevtska(-e) oblika(-e) | Rastlinska snov v prahu v trdni obliki za peroralno uporabo Rastlinska snov v prahu v poltrdni obliki za uporabo na koži |
Poročevalec(i) | I Chinou |
Recenzent | M Delbò |
OKRAJŠAVE
AGPs Arabino-galaktanske beljakovine
bid dvakrat na dan
CBMN Mikrojedro za blokiranje citokineze
CMG Chios Mastic Gum
CMW Voda iz chioske mastike
DSS Natrijev dekstran-sulfat
EROD etoksiresorufin O-detilaza
GagA s citotoksini povezan antigen
GSH Glutation
HKID Hongkonški indeks dispepsije
HP-NAP protein, ki aktivira nevtrofilce H. pylori
IL interlevkin
IMLA 24Z-izomastikadienolna kislina
IMNA 24Z-izomastikadienonska kislina
MBC Najmanjša baktericidna koncentracija
MCP-1 Monocitni kemotaktični protein-1 MIC Najmanjša inhibitorna koncentracija
MIF Zaviralni dejavnik migracije makrofagov
MMC Mitomicin-C
NOAEL ni opazne ravni neželenih učinkov
NSAIDs Nesteroidna protivnetna zdravila NF-κB Jedrski faktor-κB
oxLDL oksidirani lipoproteini nizke gostote.
PBMC mononuklearne celice periferne krvi
PDO proizvod z zaščiteno označbo porekla
PKC beljakovinska kinaza C
PMA 12-miristatni 13-acetat florbol 12-miristatni 13-acetat
SMART Test somatskih mutacij in rekombinacije tid trikrat na dan
TMEWP skupni izvleček mastike brez polimera
TNF-alfa tumorski nekrotizirajoči faktor alfa,
UBTUrea dihalni test
VacA Vacilating citotoksin A
WBC Belokrvne celice
Table of Contents
Uvod
Opis rastlinskih snovi, rastlinskih pripravkov ali njihovih kombinacij
- Rastlinska(-e) snov(-i)
V skladu s posebnim zakonom Eur. Ph. Monograph (01/2008:1876) je mastika (mastix) posušen smolnat izcedek iz stebel in vej Pistacia lentiscus L. z vsebnostjo najmanj 10 ml/kg eteričnega olja (brezvodna droga).
Mastika je oljna smola, pridobljen iz drevesa mastik (Pistacia lentiscus L.). Izrazi mastika, mastix in smola mastike se na območju Balkana uporabljajo kot sopomenke. V literaturi se pogosto imenuje tudi Chios Mastic Gum (CMG) po svojem glavnem izvoru, grškem otoku Chios.
V indijski ajurvedski farmakopeji (1999) je navedena tudi monografija smole P. lentiscus L. z imenom “Rumimastangi”. Njeno ime v različnih indijskih jezikih je naslednje:
Bengalščina: Rumi-Mastungi
Gudžaratščina: Rumi Mastagee
Hindijščina: Rumi Mastagee; Rumi Mastiki; Mastagee
Maratščina: Rumia Mastakee
Urdujščina: Rumee Mastagee
Drevo mastike (P. lentiscus L.) iz družine Anacardiaceae je naravno razširjen na območjih, ki obkrožajo obalna območja Sredozemlja, Portugalske in tropske Afrike (Gruenwald et al. 2007). Cvetovi in plodovi so kompaktni in podobni šopom. Cvetovi so rumenkasti ali vijoličasti. Oplodnica, ki je približno 4 mm velika, kroglasta, apikulasta, je rdeča, pozneje pa postane črna. Rastlina je zimzeleno dvospolno drevo ali grm, visok 1-8 m. Listi so dvopičasti. Od 8 do 12 listov meri od 1 do 5 cm na
- do 1,5 cm. So kopjasti do jajčasto kopjasti, mucronati in korikasti. Vretenica je široko krilata. Ličniki so goli (Evans, 1989).
Sinonim za P. lentiscus L. (Gennadios 1914; Rechinger 1943) je P. lentiscus var. Chia (Desf. Ex Poiret) DC, ki je uporabljen v večini obstoječih znanstvenih publikacij za to rastlino. V novejši in dobro dokumentirani botanični študiji profesorja Kazimierza Browicza je predlagano, da se namesto splošno uporabljenega botaničnega imena P. lentiscus var. Chia uporablja ime P. lentiscus cv. Chia, saj cv pomeni gojeni klon. Pred kratkim je bila vrsta P. lentiscus L. brez dodatno določene sorte ali kultivarja sprejeta v monografijo Evropske farmakopeje (Browicz 1987).
- lentiscus L. z grškega otoka Chios je komercialno med glavnimi viri mastihe (Chios Mastic Gum (CMG)) po vsem svetu s specifičnim geografskim poreklom na južnem delu otoka Chios, območje Mastihohoria (Savvidis 2000). Smola te rastline se pridobiva kot izcedek po “poškodovanju” debla in vej (Paraschos et al. 2007). Popolnoma odraslo drevo vrste P. lentiscus proizvede približno 1 kg smole na leto. Ko ta sok kaplja, je videti kot lepljiva in prosojna tekočina, ki se 15-20 dni pozneje strdi v nepravilne oblike, na katere vplivajo vremenske razmere na tem območju v poletnem času, tj. intenzivna suša in sončna svetloba. Ko se strdi, ima obliko kristalov, njegov precej grenak okus pa se hitro umiri in pusti značilno aromo.
Ko je smola pobrana, se opere z vodo, da se odstranijo nečistoče, nato pa se mastika sortira, razvrsti in klasificira glede na barvo in velikost zrnc (Dabos et al. 2010i).
Samo z otoka Chios se letno izvozi približno 250.000 kg mastike (Perikos 1986; Belles 2006); večinoma v Francijo, ZDA, Emirate, Savdsko Arabijo, Združeno kraljestvo in Avstralijo. Od leta 1997 je mastika z otoka Chios označena kot proizvod z zaščiteno označbo porekla (ZOP) na podlagi Uredbe Evropske unije št. 123/1997 (L0224/24-1-97) in je vpisana na ustrezen seznam proizvodov z ZOP Evropske unije.
O komercialni proizvodnji smole P. lentiscus iz drugih držav ni bilo na voljo nobenega dodatnega znanja.
Mastik se pojavlja v rumenih ali zelenkasto rumenih okroglih ali hruškastih solzah premera približno 3 mm. Oblika solzic zadostuje za razlikovanje od solzic sandarka (smole Tetraclinia articulata, za katero je bilo ugotovljeno, da se uporablja za njeno ponarejanje). Solze mastike so krhke, vendar pri žvečenju postanejo plastične, vonj je rahlo balzamičen, okus pa rahlo terebintinast (Evans 1989), medtem ko solze sandaraca pri žvečenju ostanejo zrnate, ne kažejo težnje po tvorbi plastične mase, imajo šibek vonj po terpentinu in nekoliko grenak okus (razlika od mastike).
Kemične sestavine
- Triterpeni (tetraciklični evfanski in dammaranski skeletni tip ter pentaciklični oleaninski in lupanski skeletni tip, kot so mastična kislina, izomastna kislina, oleanolna kislina, tirukallol itd. (Gruenwald et al. 2007).
- Monoterpenski ogljikovodiki, 20 % kisikovih monoterpenov in seskviterpenov
- Polifenoli, fitosteroli
- Naravni polimer (cis-1,4-poli-β-miren) (van den Berg et al. 1998)
Prva raziskava o kemični sestavi mastike je bila opravljena leta 1930. Vendar pa kljub razširjeni identifikaciji spojin do danes celotna sestava še ni v celoti določena. Zdi se, da je smola sestavljena iz različnih organskih sestavin, vključno z naravnim polimerom, hlapnimi in aromatičnimi sestavinami, ki sestavljajo eterično olje (mastično olje), terpenskimi kislinami, fitosteroli, polifenolnimi molekulami in velikim številom drugih potencialno aktivnih sekundarnih metabolitov, od katerih so bili nekateri prvič izolirani in določeni v naravi.
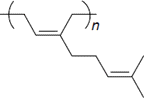
cis-1,4-poli-β-miren
Polimer mastike je bil identificiran kot cis-1,4-poli-β-miren (van den Berg et al., 1998).
Triterpenoidi v mastiki so tetraciklični evfan in dammaran ter pentaciklični olean in lupan.
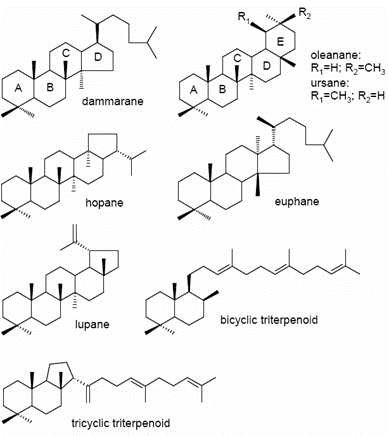
Triterpenoidi v mastiki
Nehlapni sekundarni metaboliti iz Pistacia lentiscus L., smole (mastika)
Na splošno so glavni nehlapni naravni proizvodi, o katerih poroča literatura in ki so bili izolirani iz mastike, naslednji: (a) mastikadienonska kislina, (b) tirukallol, (c) oleanolna kislina, (d) izomastikadienonska kislina, (e) 3-o-28-norolean-12-en, (f) 20(S)-3β-acetoksi-20-hidroksidammar-24-en, (g) 3-okso-dammara-20(21),24-dien, (h) 3β-hidroksimalabarica-14(26),17E,21-trien, i) 3-okso-malabarica-14(26),17E,21-trien, j) 3-β-hidroksi-28-norolean-12-en, k) 3-okso-28-norlup-20(29)-en, l) (8R)-3-Oxo-8-hidroksi-polipoda- 13E,17E,21-trien, m) 1,4-poly-β-miren (The Review of Natural Products 2005; Assimopoulou & Papageorgiou 2005i in 2005ii; Paraschos et al., 2007).
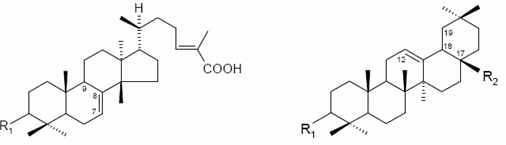
R1: O (mastikadienonska kislina)R1: O
R2: COOH (oleanolna kislina)
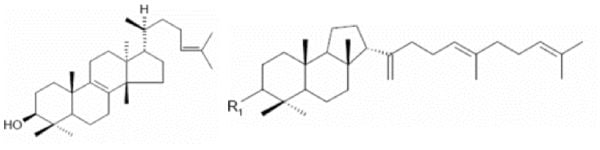
O 3-oxo-malabarica-14(26),17E,21-triene
Tirucallol
Polifenoli: Poročajo tudi o sledovih spojin tirosola, p-hidroksi-benzojske kisline, p-hidroksi-fenilocetne kisline, vanilinske kisline in galske kisline (Kaliora et al. 2004).
Hlapni sekundarni metaboliti iz Pistacia lentiscus L. (mastike in drugih delov rastlin)
V devetdesetih letih prejšnjega stoletja in v letu 2000 so bile hlapne sestavine drevesa P. lentiscus L. predmet več študij v okviru analize sestave in delovanja eteričnega olja smole (Papageorgiou et al., 1981; 1997). Leta 1991 sta Boelens in Jimenez primerjalno preučila kemično sestavo eteričnih olj smole, listov ter nezrelih in zrelih plodov mastike in ugotovila skupno 90 sestavin (50 % monoterpenskih ogljikovodikov, 20 % oksigeniranih monoterpenov in 25 % seskviterpenov) z α-pinenom (79 %) in mircenom (3 %) kot glavnima sestavinama eteričnega olja smole.
Magiatis in drugi so leta 1999 objavili obsežno študijo treh eteričnih olj mastike, listov in vej P. lentiscus L. V tej študiji so bile glavne sestavine smole α-pinen (66,48 %), mircen (8,34 %) in β-pinen (3,29 %), medtem ko so bili v eteričnem olju listov mircen (20,58 %), germacren D (13,30 %), L-kariofilen (8,33 %), α-kadinol (7,33 %) in δ- kadinen (7,00 %), v eteričnem olju vej pa mircen (47,92 %), germacren D (15,46 %) in E-kariofilen (4,75 %). Leta 2005 (Koutsoudaki et al.) so kot glavne sestavine mastihe navedli α-pinen, mircen, β- pinen, limonen in transkariofilen. Zgornje rezultate je potrdilo nedavno delo (Kokolakis et al., 2010), v katerem so avtorji opredelili iste glavne sestavine (α-pinen, mircen in β-pinen) in jih predlagali tudi kot kazalnike časa skladiščenja.
- Zeliščni pripravek(-i) Zeliščna snov v prahu
Podatki, predstavljeni v tem poročilu, izhajajo iz študij, v katerih je bila uporabljena rastlinska snov v prahu (kot edini pripravek, vključen v monografijo) ali včasih drugi pripravki mastike, kot so mastikino olje, mastikina voda ali mastikini izvlečki. Pogosto ni na voljo dovolj informacij o natančnem pripravku/moči in odmerjanju.
V literaturi se omenja tudi mastična voda (Perikos, 1986; Topitsoglou-Themeli et al., 1984; 1985; Vlastos et al., 2013). Mastikova voda je aromatična voda, ki se v velikih količinah pridobiva skupaj z mastikovim oljem med parno destilacijo mastike. Je 100-odstotni naravni vodni izvleček, ki vsebuje vse v vodi topne sestavine mastihe in majhno količino (0,5-1 % V/V) mastičnega olja.
- Kombinacije rastlinskih snovi in/ali rastlinskih pripravkov, vključno z opisom vitaminov in/ali mineralov kot sestavin ocenjenih tradicionalnih kombiniranih zdravil rastlinskega izvora, kjer je to primerno.
Informacije iz pregleda trga v zvezi s pripravki iz mastike so pokazale, da je prah široko razširjen v živilskem sektorju po vsem svetu, tudi v izdelkih za samopomoč (zobna pasta itd.) na območju Balkana in na področju kozmetike. Obstajajo tudi izdelki, v katerih se nahaja v kombinaciji. Vendar takšne kombinacije niso predmet tega poročila o oceni.
Metodologija iskanja in ocenjevanja
Ocena temelji na virih, navedenih na seznamu literature. V oceno so bile vključene tudi objave v drugih jezikih, ne le v angleščini (vsaj povzetek v angleščini ali v drugem jeziku, npr. več v grščini).
Kot iskalnik je bil uporabljen Google; ključne besede pa so bile: mastix, mastic, Pistacia lentiscus cv Chia, Pistacia lentiscus, mastic gum
Znanstvene zbirke podatkov: Scifinder, Scopus; datum iskanja avgust 2018; ključne besede: “Pistacia lentiscus cv Chia”, “Pistacia lentiscus”, “mastix”, “mastic gum”, “mastic oil”.
Za ključno besedo “mastix” ni bilo najdenih nobenih referenc.
Medicinske zbirke podatkov: Pubmed, Cochrane library; ključne besede: “Pistacia lentiscus cv Chia”, “Pistacia lentiscus”, “mastix”, “mastic gum”, mastično olje”.
Toksikološke zbirke podatkov: Toxnet; ključne besede: “Pistacia lentiscus cv Chia”, “Pistacia lentiscus”, “mastix”, “”, mastično olje”.
Viri za farmakovigilanco: Poročilo: raziskave Scopus, druge niso na voljo poročevalcu.
Drugi viri: Knjižnica Univerze v Atenah (knjižnica farmacije in farmakognozije).
Podatki o uporabi zdravil
Informacije o izdelkih na trgu
- Informacije o izdelkih na trgu v državah članicah EU/EGP
Informacije o zdravilih, ki se tržijo v EU/EGP
V Grčiji in drugih balkanskih državah se rastlinska snov “mastika” ali “” kot sopomenka pogosto uporablja v ljudskem zdravilstvu in prodaja v lekarnah, zlasti vsaj od šestdesetih let prejšnjega stoletja po mednarodnih objavah o zdravilnih učinkih mastike na prebavne motnje (funkcionalna dispepsija, kot pomoč pri zdravljenju Helicobacter pylori), zdravilne učinke na kožo in izdelke za ustno higieno.
Izmenjava informacij med regulativnimi organi EU o pripravkih iz smole P. lentiscus L. (mastike) je pokazala, da v EU/EGP ni odobrenih ali registriranih zdravil za peroralno ali kožno uporabo, ki bi vsebovala pripravke iz mastike kot posamezno zdravilno učinkovino.
Informacije o ustreznih kombiniranih zdravilih, ki se tržijo v EU/EGP
Nekateri izdelki za oromukozno uporabo (grgranje) in ustno vodo se tržijo od 50. oziroma 90. let prejšnjega stoletja (Perikos 1986; Topitsoglou et al. 1984; 1985). Za te pripravke ni na voljo posebnih informacij o jakosti in odmerjanju.
Informacije o drugih izdelkih, ki se tržijo v EU/EGP (če je to ustrezno).
Prah je že vsaj dve stoletji razširjen v živilskem in kozmetičnem sektorju po vsej Evropi. To potrjujejo izvožene količine mastike vsaj z grškega otoka Chios, ki so na voljo pri Združenju pridelovalcev mastike (Serpico 2000 in Doukas 2003, navedeno v Vlastos et al. 2013).
V Grčiji in na sredozemskem območju je znana lokalna uporaba mastičnega prahu za rane in opekline zaradi njegovih zdravilnih lastnosti (Perikos 1986; The review of natural products 2005, Paraschos et al. 2012), medtem ko se poltrdni galenski pripravek, ki vsebuje približno 10 % rastlinske snovi, pogosto uporablja v lekarnah in ga predpisujejo tudi zdravniki.
Že več let obstajajo kreme, ki vsebujejo majhen odstotek mastike v prahu (1-3 %) za kozmetične izdelke.
Informacije o izdelkih na trgu zunaj EU/EGP
Informacije o pripravkih iz smole P. lentiscus L. (mastike) in kombiniranih izdelkih so pokazale, da je prah široko razširjen v živilskem in kozmetičnem sektorju tudi v Turčiji in arabskih državah, predvsem za žensko uporabo (Al-Habbal et al. 1984). To potrjujejo izvozne količine mastihe z grškega otoka Chios, ki sta jih navedla Perikos (1986) in Belles (2006, na voljo je le povzetek) s sklicevanjem na Združenje pridelovalcev mastihe.
V Sredozemlju (Tunizija, severna Afrika), Turčiji (turški zakonik kot solut Mastix od leta 1940-1948) ter v Iranu in Iraku je znana lokalna uporaba mastičnih pripravkov za rane in opekline.
Informacije o dokumentirani medicinski uporabi in zgodovinski podatki iz literature
Zgodovinski podatki
Starogrški zdravnik Hipokrat (4. stoletje pred našim štetjem) ter pozneje Dioskorid in Galen (1. in 2. stoletje našega štetja) so prvič poročali o lastnostih chioske mastike in priporočali njeno uporabo zaradi značilnega okusa in zdravilnih lastnosti (Paraschos et al., 2007, 2012). Dokumenti kažejo, da je bil to prvi naravni žvečilni gumi v antičnem svetu, ki se je uporabljal za čiščenje zob in osvežitev zadaha. Uporabljali so ga celo v kozmetologiji za čiščenje obraza in telesa. Nato se je smola uporabljala kot aktivna sestavina v številnih farmacevtskih formulah in nostrumih, od katerih so bili številni občasno zabeleženi v mednarodnih farmakopejah (Gennadios 1914; Al-Habbal et al. 1984; Perikos 1986; Savvidis 2000).
Dioskorid (1. stoletje našega štetja) je v Materia Medica poročal o terapevtskih lastnostih mastike z otoka Chios (Chios Mastiha) in omenil, da pomaga pri prebavnih motnjah, krvnih težavah, kroničnem kašlju, hkrati pa deluje pomirjevalno. Zdravilne lastnosti žvečenja mastike je predlagal za podporo ustni higieni ter za čist in svež zadah. Omenil je uporabo olja “Mastiha”, eteričnega olja mastihe, ki se uporablja na več načinov pri obolenjih maternice in zaradi stiptičnega delovanja (Gennadios 1914).
Od 1. do 7. stoletja našega štetja so zdravniki in botaniki uporabljali mastiko predvsem za zdravljenje želodčnih motenj, kot so gastralgija, dispepsija in peptična razjeda (Paraschos et al.),
2007). Po mnenju takratnih ljudi je uporaba mastike prispevala k nemotenemu delovanju želodčnega in črevesnega sistema. Natančneje in iz različnih virov je razvidno, da so mastiko uporabljali za lajšanje bolečin v želodcu ter pri prebavnih motnjah in želodčnih težavah (Oribasij, Etius, Galen, Pilen). O učinku mastike pri atoniji in vnetju želodca, črevesja in jeter ter o mehčalnih lastnostih poroča Galen v knjigi Simpliciun medicamentorum temperamentis ac faculatibus libri XI (Perikos 1986; Belles 2006).
Jeruzalemski balzam: V lekarni frančiškanskega samostana svetega Odrešenika v Jeruzalemu, kjer je delal menih Antonio Menzani di Cuna, mu je po štiriindvajsetih letih poskusov uspelo ustvariti učinkovit balzam, imenovan “Jeruzalemski balzam” (Perikos 1986). Leta 1712 so ga v Milanu predstavili kot mazilo za zdravljenje ran, bolečin v trebuhu, dermatitisa, črevesnih črvov, zobobola, hemoroidov itd. Menzanijeva formula je vsebovala štiri sestavine: aloe, kadilo, miro in mastiko, raztopljene v etanolu. Gilbertus Anglicus (13. stoletje v Angliji) je v svojem Compendium Medicinae nostrum za vranico imenoval “diacerasus”, ki vsebuje češnjev sok, cimet in mastiko. Pozneje je Giovanni de Vigo, frančiškanski menih in zdravnik papeža Julija II., predpisal balzam za srbečico, ki je vseboval jajčni beljak, laneno seme, topolove popke in mastiko v prahu v oljčnem olju (Perikos, 1986). Nekatere različice formule so vključene v nekatere farmakopeje (B.P., 1998 (ni na seznamu literature). Martindale: The Extra Pharmacopeia, 33. izdaja, navedena v Moussaieff et al. 2005).
Več kot 250 let se je formula, najdena v rokopisu nekega samostana, ki vsebuje štiri rastline: olibanum (Boswellia spp.), miro (Commiphora spp.), aloe (Aloe sp.) in mastiko (P. lentiscus L. gum) (16:3:9:12), očitno pogosto uporabljala in se zaradi protivnetnih, zdravilnih, antioksidativnih in protiseptičnih lastnosti uporablja še danes.
Paracelsus je v svoji knjigi Der grossen Wundartzney (Velika knjiga o kirurgiji) predlagal mastično smolo za “celjenje ran”. V 18. in 19. stoletju so mastično smolo uporabljali za zapolnjevanje zobnih votlin, tako da so v bučki raztopili 4 dele mastične smole in 1 del etra: z raztopino rumenkaste barve in oljnate konsistence so navlažili vatirano palčko in jo nanesli na votlino, da bi jo zapolnili in zatesnili. Te načine uporabe mastihe so ohranili tradicionalni zdravilci vzhodnega Sredozemlja in Bližnjega vzhoda, kjer je uporaba mastihe izredno razširjena. Poleg tega so Al-Razi, Abu Yusuf Ya’qub ibn Ishaq al-Kindi in Abu Marwan’Abd al-Malik predpisali mešanice v medicinskih formulah za zapolnitev pokvarjenih zob, okrepitev želodca, pomoč jetrom (Perikos 1986, Belles 2006; Al-Habbal et al. 1984).
V začetku 20. stoletja so v več člankih poročali o “Mastisolu”, pripravku iz mastike, ki se je uporabljal za celjenje ran, z nekoliko drugačno sestavo, ki se razlikuje od današnjega Mastisola, ki se uporablja kot tekoče lepilo (in vsebuje mastiko, stiraks, metil salicilat in alkohol). Glede na navedbe so Mastisol in njegovi nadomestki (analogni) smolnate raztopine, podobne sluzi (McDill 1918), ki se nanesejo na prizadeto območje in pustijo izhlapevati, dokler nanos ne postane lepljiv. Nato se lahko (ali pa tudi ne) nanese povoj in ostane na mestu, dokler ne pride do ozdravitve, razen če pride do gnitja in se v tem primeru zdravilo obnovi (The Merck’s Annual Report 1913, Shaw 1914, McDill 1918). Pri tej metodi je bilo v primerjavi z drugimi antiseptičnimi oblogami za rane ugotovljenih več prednosti, zaradi katerih je bila med vojnami priljubljena tudi v terenskih bolnišnicah: Izogibanje vsem postopkom čiščenja, ki so škodljivi za rane in povzročajo bolečine; neodvisnost od vode, s čimer se izognemo vlagi, ki je tako ugodna za rast bakterij; velika preprostost postopka, ki se ga zlahka naučijo laiki; velik prihranek časa; lahko se uporablja na tistih delih telesa, na katere je težko namestiti povoje; povoja ni mogoče premakniti; poceni; manjše draženje kože v primerjavi z drugimi razkužili, kot je jod; varnost pred okužbo, saj asepsa, dosežena z mastičnim povojem, traja zelo dolgo časa. Poleg tega jo je mogoče enostavno pripraviti v bolnišnicah (The Merck’s Annual Report 1913, Shaw 1914, McDill 1918).
V Merckovem letnem poročilu za leto 1913 je Mastisol naveden kot smolnat pripravek, ki vsebuje 5 % mastike (terebinta 15 g, mastike 12 g, smole (katere koli) 25 g, smole alb. 8,0 g, alkohol 90 % 180 g), ki ga je kot oblogo za rane priporočil doktor von Oettingen iz Berlina kot direktor nemške terenske bolnišnice v balkanski vojni, ki je spremenil prejšnjo formulo, ki jo je leta 1900 s tajnim lastniškim pripravkom uvedel ortopedski kirurg. American Review of reviews (Shaw 1914) poroča, da je isti nemški kirurg von Oettingen v rusko-japonski vojni za antiseptično obdelavo ran uporabljal raztopino 20 g mastike v 50 g kloroforma in 20 kapljicah lanenega olja, medtem ko so v balkanskih bolnišnicah v isti namen uporabljali raztopino mastike v benzolu.
Krebser je za zdravljenje operativnih ran uporabljal formulo, ki je vsebovala približno 28 % mastike (20 g mastike, razredčene v 50 g kloroforma, z dodatkom 1 g lanenega olja) (The Merck’s Annual Report 1913).
Suter je uspešno uporabljal mastisol za zdravljenje operativnih ran, Wagner pri zdravljenju ran, Naugebauer pa pri opeklinah in koroziji (Merckovo letno poročilo 1913).
Poleg tega je McDill v medicinskem vojnem priročniku št. 5 “Lessons from the Enemy How Germany cares for her war disabled” poročal o isti formuli, ki je vsebovala približno 28 % mastike (mastike 20 g, 50 g in lanenega olja 20 kapljic) kot sluzi, ki se uporablja kot kirurška obloga (McDill 1918).
V knjižici “The chemist and Druggist” št. 1818, letnik LXXXV, november 1914, je navedena obloga za rane Mastisol in njena zgodovinska uporaba. Poroča se, da se v Nemčiji uporablja od leta 1913 (Pharmaceutisch Weekblad, 1913, str. 104) kot zdravilno sredstvo v formuli (kot imitacija mastisola), ki vsebuje približno 4 % mastike (mastik 2 g, benzol 50 g, neznan eter 20 kapljic). Druge formule za mastisol navaja “Pharm. Ztg.”, kjer je ponovno omenjena raztopina 20 g mastike v 50 g kloroforma z dodatkom 20 kapljic lanenega olja (približno 28 % mastike), in Nordmann, ki predlaga 20 g mastike, 50 g benzola, 20 kapljic lanenega olja, 10 g kolofonije in 7 g beneškega terpentina (približno 23 % mastike) (The chemist and Druggist 1914).
Te formule za mastisol so se uporabljale tudi pozneje. V turškem zakoniku (1940-1948) je mastisol naveden kot fantazijsko ime pripravka Mastix solutus (Sakiz mahlolu), ki vsebuje 28 % mastikove smole (28 g mastike, 71 g benzola, 1 g lanenega olja). To ustreza pripravku, ki so ga uporabljali v balkanskih bolnišnicah in ga je navedel Shaw (1914) v American Review of reviews. O isti raztopini, ki vsebuje 28 % mastike v benzolu in lanenem olju, poroča tudi Medicamenta, italijanski teoretično-praktični priročnik za zdravstvene delavce (zdravnike in farmacevte (Medicamenta 1965).
Sollman (1957) ponavlja, da se je več formul, ki vsebujejo mastiko, uporabljalo kot kirurški lak za fiksiranje kožnih bakterij na rokah in operativnem področju. Med njimi navaja Borchatovo, ki vsebuje 40 % mastike v organskem topilu (40 g mastike, 60 g benzola, 20 kapljic ricinusovega olja).
Knjiga Perikos 1986 navaja zdravilne lastnosti mastične kreme (patentirane leta 1958 s strani izumitelja S. Paradeisopoulosa), ki vsebuje 10-20 % pistacijeve smole/praška, proti vsem vrstam poškodb kože (kot so opekline, vojne rane, furunkli, luskavica, dermatološke bolezni itd.) Obstaja korespondenca med izumiteljem in Združenjem pridelovalcev mastike ter objave v časopisih Press of in grških časopisih.
Mastiko so orientalske ženske tradicionalno uporabljale kot sredstvo za žvečenje (British Pharmaceutical Codex 1949, citirano v Al-Habbal et al. 1984) in sladilo za dihanje ter kot sestavino sladkarij in pijač (Tanker & Tanker, citirano v Al-Habbal et al. 1984). Mastik sam ali alkoholne raztopine se uporabljajo v zobozdravstvu za polnjenje karioznih zob (Wren 1971, British Pharmaceutical Codex 1949; Martindale Extra Pharmacopoeia 1978, citirano v Al-Habbal et al. 1984). Poleg tega se uporablja (Pigmentum Mastiche Compositum) kot kirurški lak za zaščito ran (Martindale Extra Pharmacopoeia
1978, citirano v Al-Habbal et al. 1984). V literaturi doslej niso bili omenjeni nobeni neželeni učinki široke uporabe mastike.
Merckov indeks, 10. izdaja. 1983 navaja uporabo mastike kot zobozdravstvenega pripomočka v zobnih cementih, obližih, lakih, žvečilnih gumijih in kadilih (The Merck Index 1983).
Medicamenta 8. izd. 1965 navaja mastiko za notranjo uporabo kot infuzijo (2-8 g dnevno) kot tonik in adstringent (pri otroški diareji), za žvečenje in sestavine zobnih cementov, ki vsebujejo različne formule, v katerih se mastiko raztopi v organskih topilih (zaradi njene netopnosti v vodi), raztopina pa se lahko absorbira na glini ali drugi podlagi (Medicamenta 1965).
Številni zdravniki, farmacevti in botaniki so se sklicevali na terapevtske lastnosti mastične smole, ki so jo uporabljali za pripravo terapevtskih formul in široko uporabljanih pripravkov. Uporaba mastike se je uspešno širila tudi v bizantinskih časih. Od prejšnjega stoletja se mastika uporablja kot začimba v sredozemski kuhinji, pri proizvodnji žvečilnih gumijev, v parfumeriji, zobozdravstvu in pri lokalnem prebivalstvu otoka Chios za lajšanje bolečin v epigastriju in zaščito pred peptično razjedo (The Review of Natural Products 2005; Al-Habbal 1984). Več avtorjev je v osemdesetih letih prejšnjega stoletja menilo, da so danes potencialne terapevtske dejavnosti mastike znanstveno raziskane, in pokazali, da zlasti mastik z grškega otoka Chios (na katerega se je nanašala večina študij) pozitivno deluje proti prebavnim motnjam, prispeva k ustni higieni, deluje protimikrobno in protivnetno, je naravni antioksidant in lahko pomaga pri celjenju poškodb (Topitsoglou-Themeli et al. 1984; 1985; Al-Habbal et al. 1984; Huwez & Al-Habbal 1986).
Poročali so, da mehanizem delovanja mastike pri lajšanju simptomov in zdravilnih lastnostih ni znan. Ker pa mastika ni topna v vodi, so domnevali, da je mogoče, da tvori komplekse z beljakovinami in ustvarja citoprotektivno plast, ki dodatno ščiti želodčno sluznico in kožne rane. Ta hipoteza lahko pojasni različne uporabe mastihe (pigmentum mastiche compositum) kot kirurškega laka za zaščitno prekrivanje ran (Huwez in Al-Habbal 1986).
Vrsta poročil v mednarodnih medicinskih revijah potrjuje zgodovinsko zabeležene lastnosti mastike, ki temeljijo na rezultatih laboratorijskih študij in manjših kliničnih preskušanj, ki so jih izvedli neodvisni raziskovalci v Grčiji in tujini, ter kažejo, da ima mastikova smola zanimive bioaktivne lastnosti. (Al Habbal et al. 1984; Al Said et al. 1986; Huwez et al. 1986; 1998; Perrikos 1986; Dabos et al. 2010i; 2010ii; Kaliora et al. 2007i; 2007ii).
Trenutne raziskave kažejo, da imata mastika (glede na dosedanje študije predvsem z otoka Chios, CMG) in njeno eterično olje protimikrobne in antioksidativne lastnosti. Antibakterijsko delovanje (Magiatis et al., 1999; Iauk et al., 1996; Koutsoudaki et al., 2005) in njeno delovanje in vivo proti plakom v ustni votlini so pripisali njenemu zaviralnemu delovanju na splošno rast bakterij (Takahashi et al., 2003), zlasti proti Streptococcus mutans in Helicobacter pylori (Aksoy et al., 2006).
Za peroralno uporabo proti težavam s prebavili je priporočeni odmerek, ki temelji na tradiciji mastike v prahu, po Perikosu (1986) 0,5-1 g mastike v prahu kot enkratni odmerek, do 2-krat na dan, trajanje 2-krat na dan (dnevni odmerek 1-2 g).
Mastiko so v manjših kliničnih preskušanjih uporabili tudi Al-Habbal in drugi (1984) ter Huwez in Al-Habbal (1986). Dnevni odmerek je v skladu z eno študijo (Huwez & Al-Habbal, 1986) do 2 g. Te klinične študije so bile izvedene v državah zunaj EU za drugo indikacijo (razjeda dvanajstnika ali želodca) in so uporabljale drugo doziranje. Zato se lahko rezultati štejejo za podporne le z vidika varnosti.
V Indijski ajurvedski farmakopeji (1999) je tudi monografija, ki omenja smolo
- lentiscus L., imenovan “Rumimastangi”, in njegova uporaba v zdravilne namene je bila predlagana v dnevnem odmerku 1-2 g, ki je primerljiv z odmerki, ki se uporabljajo v Evropi.
Za uporabo na koži se mastikin prah že stoletja uporablja kot zdravilno sredstvo na koži ali na obližih in oblogah (Perikos 1986, The Review of natural products 2005; Paraschos et al. 2012). Od leta 1912 obstajajo navedbe o uporabi mastike, razredčene v organskih topilih, pri poškodbah kože, hudih kožnih ranah itd (The Merck’s Annual Report 1913; The Chemist and Druggist 1914, Shaw 1914, Sollmann 1957).
Obstajajo tudi galenske formule (poltrdni pripravki), ki jih pripravljajo v lekarnah in se pogosto uporabljajo (predpisujejo jih tudi zdravniki) ter so znane po svojih zdravilnih namenih.
Preglednica 1: Pregled preteklih podatkov
| Zeliščni pripravek | Dokumentirana uporaba / Tradicionalna uporaba | Farmacevtska oblika, Moč Pozologija Trajanje uporabe | Referenca |
| Mastika v prahu | Za prevezovanje ran, zdravljenje operativnih ran, ran, opeklin in korozij druge in tretje stopnje. | Smolna raztopina ≈28 % mastike v organskem topilu (20 g mastike, 50 g kloroforma in 1 g lanenega olja) | Merckovo letno poročilo 1913 |
| Mastika v prahu | Obloga za rane | Smolna raztopina Različne formule: npr. kapljic lanenega olja) ≈23 % mastike v organskem topilu (20 g mastike, 50 g benzola, 20 kapljic lanenega olja, 10 g kolofonije in 7 g beneškega terpentina) 20 % mastike v organskem topilu (mastik 20 delov, kolofonije 20 delov, ricinusovega olja 3 dele, metil salicilata 1 del in benzola 56 delov) Kožna uporaba | The Chemist and Druggist 1914 |
| Mastika v prahu | antiseptično zdravljenje ran | Smolna raztopina ≈28 % mastike v organskem topilu (20 g mastike, 50 g kloroform, 20 kapljic lanenega olja) (ali mastik v benzolu) Kožna uporaba: Za nanos barve na prizadeto območje | Shaw 1914 Ameriški pregled pregledov |
| Mastika v prahu | Kirurška obloga | Raztopina kot sluz (imenovana mastisol) ≈28 % mastike v organskem topilu (mastike 20 g, benzol 50 g, laneno olje 20 kapljic) Kožna uporaba: Za nanos barve na prizadeto območje | McDill 1918 |
| Mastika | Ni določeno | 28 % mastike v organskem topilu (mastik 28 g, benzol 71 g, laneno olje 1 g) Kožna uporaba | Turški zakonik kot (od leta 1940-1948), Medicamenta 1965 |
| Mastika v prahu | Tradicionalna uporaba, ljudsko zdravilo za gastrointestinalne motnje/lahke dispeptične/gastrointestinalne motnje | Peroralna uporaba: 0,5-1 g dvakrat na dan Trajanje uporabe: 2-4 tedne | Perikos 1986 |
| Mastika v prahu | Želodčna razjeda | Peroralna uporaba Dnevni odmerek: 1 g | Pregled naravnih proizvodov 2005 |
| Mastika v prahu | Tradicionalna uporaba pri vnetjih, črevesnih motnjah, izgubi apetita | Peroralna uporaba Dnevni odmerek: 1-2 g | Ajurvedska farmakopeja Indije 1999 |
| Mastika |
| Peroralna uporaba: 2-8 g dnevno v obliki infuzije | Medicamenta 1965 |
| Mastika v prahu | Tradicionalna uporaba, ljudsko zdravilo za simptomatsko zdravljenje manjših vnetij v ustih | Oromukozna uporaba V raztopinah za grgranje/zobnih pastah Dnevni odmerek ni ustrezno opredeljen | Perikos 1986 Topitsoglou-Themeli et al., 1984 |
| Eterično olje mastike | Tradicionalna uporaba, ljudsko zdravilo za simptomatsko zdravljenje manjših vnetij v ustih | Oromukozna uporaba Dnevni odmerek ni ustrezno opredeljen | Perikos 1986 Topitsoglou-Themeli |
| Mastikova voda | Tradicionalna uporaba, ljudska raba zdravilo za simptomatsko zdravljenje manjših vnetij v ustih | Oromukozna uporabaV raztopinah za grgranje/zobnih pastah Dnevni odmerek ni ustrezno opredeljen | Topitsoglou-Themeli et al., 1984; 1985 |
| Mastika v prahu | Tradicionalna uporaba, ljudsko zdravilstvo za simptomatsko zdravljenje manjših vnetij kože in kot pomoč pri celjenju manjših ran | Galenski poltrdni pripravki, ki vsebujejo prah lentiscus L. smola (mastik 9-11 %, večinoma 10 %) Večkrat na dan na prizadeto območje kože | Galenski pripravki (kopije iz lekarniških zvezkov in knjig receptov ter zdravniških receptov; ni na seznamu literature) |
| Mastika v prahu | zdravilne lastnosti proti več vrstam poškodb kože (kot so opekline, vojne rane, furunkli, dermatološke bolezni itd.) | Patentirana krema za dermatološka obolenja, ki vsebuje 10-20 % mastike kožna uporaba | Perikos 1986 (patent od leta 1958) |
| Mastika | Sestavni del zobnih cementov | Različne formule, ki vsebujejo kit v organskih topilih (in glino ali drugo podlago za cement) | Medicamenta 1965 |
Splošne ugotovitve o uporabi zdravil
Od konca sedemdesetih let prejšnjega stoletja do začetka osemdesetih let prejšnjega stoletja se je v medicinske namene uporabljal prah smole
- lentiscus L. je zaradi svojih zdravilnih lastnosti postal priljubljen v tradicionalni medicini v Grčiji, sredozemskih in azijskih državah (Bližnji vzhod) ter v ZDA. Na voljo je več podpornih virov s podrobnostmi o moči, odmerjanju in indikacijah za oralno in kožno uporabo.
Preglednica 2a: Pregled dokazov o obdobju uporabe zdravil (oralna uporaba)
| Zeliščni pripravek/farmacevtska oblika | Navedba | Pozologija, moč | Obdobje uporabe zdravila |
| Mastik v prahu | Tradicionalna uporaba, ljudsko zdravilo za prebavne motnje/lahek dispeptik/ prebavila | Peroralna uporaba 0,5-1,g, dvakrat na dan Trajanje uporabe: 2-4 tedne | Perikos 1986 |
Zahteve za obdobje uporabe zdravila v skladu z Direktivo 2001/83/ES v zvezi s “tradicionalno uporabo” pri peroralni uporabi se štejejo za izpolnjene za naslednje indikacije:
- Tradicionalno zdravilo rastlinskega izvora, ki se uporablja pri blagih dispeptičnih motnjah
Na podlagi razpoložljivih literaturnih virov je predlagana naslednja pozologija za peroralno uporabo praška:
- Enkratni odmerek: 0,5-1 g
- Dnevni odmerek: 1,0-2 g
- Trajanje uporabe: Če se tovrstni simptomi med uporabo zdravila pojavljajo dlje časa, se je treba posvetovati z zdravnikom ali usposobljenim zdravstvenim delavcem (skladno z drugimi zdravili rastlinskega izvora z enakimi indikacijami).
Preglednica 2b: Pregled dokazov o obdobju uporabe zdravila (kožna uporaba)
| Zeliščni pripravek Farmacevtska oblika | Navedba | Pozologija, moč | Obdobje uporabe zdravila |
| Mastika v prahu | Za prevezovanje ran, zdravljenje operativnih ran, ran, opeklin in korozij druge in tretje stopnje | Smolna raztopina | Merckovo letno poročilo 1913 |
| Mastika v prahu | Antiseptično zdravljenje ran | Smolna raztopina | Shaw 1914 Ameriški pregled pregledov |
| Mastika v prahu | Obloga za rane | Smolna raztopina Kožna uporaba: ≈28 % mastike v organskem topilu (20 g mastike, 50 g kloroforma in 20 kapljic lanenega olja) | The Chemist and Druggist 1914 |
| Mastika v prahu | Kirurška obloga | Raztopina kot sluz (imenovana mastisol) Za nanos barve na prizadeto območje | McDill 1918 |
| Mastika v prahu | Za dermatološka obolenja (v zdravilne namene) (osebna komunikacija s prof. F. Demircijem) | Smolna raztopina (imenovana mastix solute ali mastisol) Zunanja uporaba Mastik 28 % v organskih topilih (mastik 28 g, benzol 71 g, laneno olje 1 g) | Turški zakonik (od leta 1940-1948) Medicamenta 1965 |
| Mastika v prahu | Pri operaciji za pritrditev kožnih bakterij na rokah in operativnem območju | ≈40 % v organskih topilih (mastik 40 g, benzol 60 g, ricinusovo olje 20 kapljic) Uporaba na koži: kot lak, ki se nanese s čopičem in posuši | Sollmann 1957 |
| Mastika v prahu | Tradicionalna uporaba, ljudsko zdravilstvo za simptomatsko zdravljenje manjših vnetij kože in kot pomoč pri celjenju manjših ran | Galenic Poltrdni pripravek, ki vsebuje prah P. lentiscus smola (mastik 9-11 %, večinoma 10 %). Večkrat na dan na prizadeto območje kože | Galenski pripravki (kopije iz lekarniških zvezkov in knjig receptov ter zdravniških receptov; ni na seznamu literature) |
| Mastika v prahu | Zdravilne lastnosti proti več vrstam poškodb kože (kot so opekline, vojne rane, furunkli, dermatološke bolezni itd. | Patentirane kreme, ki vsebujejo 10-20 % mastike za dermatološka obolenja | Perikos 1986 (patent S Paradeisopoulos od leta 1958) |
Kožna uporaba
Zahteve za obdobje uporabe zdravila v skladu z Direktivo 2001/83/ES v zvezi s “tradicionalno uporabo” se štejejo za izpolnjene za kožno uporabo za naslednje indikacije:
- Tradicionalno zdravilo rastlinskega izvora, ki se uporablja za simptomatsko zdravljenje manjših vnetij kože in kot pomoč pri celjenju manjših ran
Kožna medicinska uporaba mastike je utemeljena z njeno splošno in stalno uporabo kot antiseptičnega zdravila pri celjenju ran in za kirurške obloge v več pripravkih v Evropi (od leta 1912) in zunaj EU (od leta 1918 v ZDA, od leta 1940 v Turčiji). Uporaba v medicini se nanaša na pripravke, ki vsebujejo različne koncentracije (najbolj omenjena je ≈28 %) mastike, raztopljene v organskih topilih (zaradi njene netopnosti v vodi), ki danes niso dovoljeni za uporabo v medicini zaradi njihove toksičnosti. Namen uporabe organskih topil je bil tudi ta, da se omogoči njihovo izhlapevanje, preostala lepljiva plast mastike pa bi lahko služila tudi kot lepilo za povoje, vendar bi jo lahko preprosto nanesli na majhne rane na rokah, prstih in obrazu, ki bi ostale v položaju brez vezave zdravila (The Merck’s Annual Report 1913, Shaw 1914, McDill 1918).
Galenski (magistralni) pripravek, ki se trenutno uporablja, se nanaša na nižjo koncentracijo (večinoma okoli 10 %), ki jo je mogoče doseči z drugimi topili ali večinoma olji (npr. v kremah). Ta tradicionalna uporaba je dokazana z zdravniškim receptom, pa tudi z lekarniškimi knjigami ali recepti (na seznamu literature ni navedbe). O večstoletni uporabi mastike v zdravilnem mazilu poročajo tudi Paraschos et al. 2012, pri čemer se sklicujejo na stare recepture in stare farmakopeje. Vlagatelj vloge za registracijo mora izbrati najprimernejšo pomožno snov za izdelek, ki bo dan na trg, in po potrebi izvesti študije lokalne tolerance za kožni pripravek.
Ker člen 16c(c) Direktive 2001/83/ES zahteva dokumentirano medicinsko uporabo v obdobju najmanj 30 let, od tega najmanj 15 let v EU, kar je izpolnjeno tudi, če trženje izdelka ni temeljilo na posebnem dovoljenju, se lahko podatki v zvezi s temi izdelki uporabijo za utemeljitev tradicionalne uporabe kožnih pripravkov iz mastike.
Za kožno uporabo mastike predlagamo naslednjo pozologijo:
Poltrdni pripravek, ki vsebuje 9-11 %1 mastike v prahu. Do 3-krat na dan.
Trajanje uporabe: 1 teden, nanesite v tankem sloju na prizadeto področje kože.
Zgoraj navedeno trajanje uporabe je predlagano glede na to, da je izdelek namenjen samozdravljenju, in če se tovrstni simptomi med uporabo zdravila nadaljujejo ali poslabšajo, se je treba posvetovati z zdravnikom ali usposobljenim zdravstvenim delavcem.
Neklinični podatki
Pregled razpoložljivih farmakoloških podatkov o rastlinski(-ih) snovi(-ah), rastlinskem(-ih) pripravku(-ih) in ustreznih sestavinah Primarna farmakodinamika
Študije in vitro
Protimikrobna aktivnost mastike, mastikovega olja in drugih pripravkov
Izvedenih je bilo več študij, v katerih so preučevali protimikrobne lastnosti mastike.
Različne pripravke listov P. lentiscus L. (10 % poparek, ekstrakt petroleterja, ekstrakt etanola, infuzija in maceracija) smo testirali proti izbranim grampozitivnim (+) in gramnegativnim (-) bakterijam, vendar je le poparek pokazal določeno aktivnost (MIC 312 mg/ml), medtem ko so bili vsi štirje drugi pripravki praktično neaktivni proti S. lutea, S. aurea in E. coli (Iauk 1996).
Daifas in drugi (2004) so preučevali vpliv mastične smole in njenega eteričnega olja, samostojno in skupaj z etanolom, na rast proteolitičnih sevov Clostridium botulinum v mediju in na proizvodnjo nevrotoksina v študijah izzivanja z angleškimi drobtinami. Preliminarne študije z uporabo metode “spot-on-the-own” so pokazale, da so bile za popolno inhibicijo vseh testiranih sevov C. botulinum potrebne visoke ravni mastične smole v etanolu (~8 % m/m), vendar je imela mastična smola v etanolu večji protibotulinski učinek kot sam etanol. Za inhibicijo proteolitičnih sevov C. botulinum pa so bile potrebne le nizke vsebnosti mastičnega olja (~0,3 % m/m). Obe študiji sta pokazali inhibicijo, specifično za sev, z
sevi C. botulinum tipa A so bolj občutljivi na mastično smolo in njeno eterično olje kot sevi tipa B. Vendar se je mastična smola v etanolu izkazala za učinkovitejšo, če je bila uporabljena kot inhibitor v parni fazi, nanesen na bombažne blazinice in položen v inokulirane plošče, kot če je bil dodan neposredno v medij. Medtem ko sta mastična smola in njeno eterično olje zavirala rast proteolitičnih sevov C. botulinum in vitro, nista zavirala proizvodnje nevrotoksina v študijah z izzivanjem C. botulinum v angleških drobtinah.
Protibakterijsko delovanje eteričnega olja mastike je bilo preizkušeno z različnimi rezultati. Tassou in Nychas (1995) sta ugotovila določeno aktivnost pri Gram-pozitivnih sevih, vendar nobene pri Gram-negativnih. Magiatis in drugi (1999) so poročali o določeni aktivnosti eteričnega olja iz smole, ne pa tudi iz listov ali vejic, in jo pripisali predvsem α-pinenu. Koutsoudaki in drugi (2005) so to pripisali kombinaciji več sestavin in predlagali, da te delujejo sinergistično glede na to, da so različne bakterije občutljive ali neobčutljive na različne spojine eteričnega olja.
1 Opomba: Čeprav reference morda kažejo na širšo možno moč, je treba to ponovno preučiti ob naslednji sistematični reviziji monografije.
Baktericidni učinek mastihe, mastičnega olja ali frakcij/sestavin mastihe na Helicobacter pylori
Številne študije so pokazale, da mastika in mastično olje delujeta na poškodbe prebavil. Po odkritju bakterije Helicobacter pylori in povezavi z boleznimi prebavil leta 1983 se je zanimanje za določitev mehanizma delovanja mastike in mastikovega olja pri teh boleznih osredotočilo na raziskovanje in morebitno ugotovitev lastnosti proti bakteriji Helicobacter pylori.
Prvo poročilo o delovanju mastike proti H. pylori je bilo objavljeno v reviji New England Journal of Medicine v dopisu uredniku (Huwez et al., 1998). Izkazalo se je, da mastika uničuje sev H. pylori NCTC 11637 in šest kliničnih izolatov. V posebni študiji so bili uporabljeni sveži vzorci s prisotnostjo
- pylori, ki so jih izolirali od bolnikov, in poiskali najmanjšo baktericidno koncentracijo (MBC) mastihe, kar pomeni najmanjšo koncentracijo, ki je potrebna za uničenje 99,9 % bakterije v 24 urah. Mastik je uničil bakterijo v vseh pregledanih vzorcih, ne glede na velikost populacije. MBC mastihe je bila 60 μg/ml, vendar je bilo antibakterijsko delovanje opaženo tudi pri manjših koncentracijah.
Marone et al. (2001) in Bona et al. (2001) sta ocenila antibakterijski učinek mastike na klinične izolate H. pylori v koncentracijah od 2000 do 1,9 µg/ml. MBC, izračunane z metodo mikrodilucije, so pokazale, da mastika izkazuje izjemen baktericidni učinek na 12 sevov H. pylori, izoliranih od bolnikov, pri čemer je v koncentraciji 125 μg/ml uničila 50 % vodilnih, v koncentraciji 500 μg/ml pa 90 %. Poleg tega je mikroskopsko opazovanje morfologije bakterij z elektronsko emisijo pripeljalo do zaključka, da smola povzroča sproščanje zračnih mehurčkov, izziva morfološke anomalije in segmentacijo celic H. pylori. Baktericidno lastnost mastike na H. pylori so poskušali umestiti tudi v arabino-galaktanske beljakovine (AGP), izolirane iz smole (Kottakis et al., 2009). Natančneje, preučevali so zaviranje rasti H. pylori v prisotnosti vodnih izvlečkov mastike, ki vsebujejo AGP. Rezultati so pokazali, da so bili izvlečki z najmanj
1,4 g smole vpliva na sposobnost preživetja bakterij in preprečuje rast celic. Ni bilo znakov, da AGP povzročajo nenormalno morfologijo pri H. pylori, kot je bilo omenjeno za celotno mastiko (Bona et al., 2001).
Paraschos in drugi (2007) so uporabili uveljavljen model okužbe s H. pylori, da bi ocenili potencialni terapevtski učinek stalnega dajanja celotnega ekstrakta mastike brez polimera (TMEWP) na kolonizacijo s H. pylori in razvoj z njim povezanega gastritisa. Sprva je bil TMEWP pridobljen iz surove mastike v 70-odstotnem deležu, nato pa je bil razdeljen na dve frakciji, kislo in nevtralno. Kisla frakcija TMEWP je po kromatografskih ločitvah vsebovala glavne triterpenske kisline oleanonsko kislino (515 mg), moronsko kislino (338 mg), 24Z-masticadienonsko kislino (1,1 g), 24Z-izomastikadienonsko kislino (1,0 g), 24Z-masticadienolsko kislino (95 mg) in 24Z-izomastikadienolsko kislino (102 mg). Nevtralna frakcija je po podobni obdelavi vsebovala pet nevtralnih triterpenskih spojin: tirukallol (110 mg), dammaradienon (128 mg), 28-norolean- 12-en-3-on (206 mg), oleanonski aldehid (152 mg) in oleanolni aldehid (98 mg). Nato smo tri mesece testirali protimikrobno delovanje vseh teh frakcij in celotnega ekstrakta mastike proti skupini 10 kliničnih izolatov H. pylori in referenčnemu sevu CCUG 38771. Izvlečki mastihe so pokazali baktericidno delovanje, odvisno od koncentracije in seva. Natančneje, pri vseh testiranih sevih je kisla frakcija pokazala največjo aktivnost s povprečno MBC 0,136 mg/ml, sledil je TMEWP (MBC 0,256 mg/ml). Manjšo aktivnost je imela nevtralna frakcija TMEWP (0,638 mg/ml). Med posameznimi testiranimi sevi so bile ugotovljene do dvakratne razlike v MBC, le pri sevu LAVHP-7 je bila opažena večja občutljivost za TMEWP in njegovo kislo frakcijo. Ker je bila najvišja aktivnost dosežena s kislo frakcijo TMEWP, so avtorji nadaljevali s testiranjem izoliranih čistih kislih spojin na antihelikobakterijsko aktivnost. Najvišjo skupno aktivnost so dosledno in za vseh 11 testiranih sevov H. pylori dosegli z izomastikadienolno kislino s povprečno MBC 0,202 mg/ml (0,443 mM), ki ji je sledila mastikadienolna (0,220 mg/ml [0,482
mM]), oleanonsko (0,292 mg/ml [0,643 mM]) in moronsko kislino (0,310 mg/ml [0,683 mM]). Zanimivo je, da so 3-okso derivati, izomastikadienonska in mastiikadienonska kislina, pokazali manjšo aktivnost v primerjavi z ustreznimi 3-hidroksilnimi derivati. Potrjeno je bilo, da je kemijska sestava TMEWP praktično enaka sestavi surove mastihe, razen odsotnosti polimera, ter da ima tudi boljše lastnosti topnosti in večjo koncentracijo aktivnih sestavin. Poskusi so pokazali, da lahko celotni izvleček mastike zmerno zmanjša kolonizacijo H. pylori v predelu in telesu želodca. Izračunano zmanjšanje ravni kolonizacije je bilo približno 30-kratno. Ti rezultati so se ujemali z vidnim zmanjšanjem kolonizacije H. pylori, opaženim pri histopatoloških ocenah. Po mnenju avtorjev rezultati kažejo tudi na to, da bi lahko bilo običajno dolgotrajno uživanje mastike učinkovito pri zmanjševanju kolonizacije H. pylori.
Po zgornji študiji so Kottakis in drugi (2009) preučevali učinek AGP (arabino-galaktanske beljakovine), pridobljenih iz mastike iz Chiosa (CMG), in vitro in in vivo, v prisotnosti nevtrofilno aktivirajoče beljakovine H. pylori (HP-NAP), na notranje aktivatorje celične imunosti (aktivatorje nevtrofilcev), pri čemer so primerjali bolnike nosilce H. pylori z zdravimi prostovoljci, ki so dva meseca prejemali 1 g smole dnevno. Dejavniki virulence H. pylori so trije ohranjeni antigeni, in sicer nihajoči citotoksin A (VacA), s citotoksinom povezani antigen (GagA) in HP-NAP. VacA sodeluje z membrano epitelijskih celic in vstopi vanjo, kjer tvori ionski kanal z nizko prevodnostjo. Znano je, da HP- NAP privlači in aktivira nevtrofilce, monocite in mastocite, kar povzroči sproščanje pro-vnetnih mediatorjev. V tej študiji so poskusi s potegom na površje prvič pokazali specifično vezavo AGP na dve membranski beljakovini nevtrofilcev, kar lahko povzroči zaviranje aktivacije nevtrofilcev. Čeprav ti dve beljakovini nevtrofilov v tej študiji nista bili karakterizirani, avtorji navajajo, da so potrebne nadaljnje študije za razjasnitev njunih značilnosti in vpletenosti v dejavnosti nevtrofilov. Pri H. pylori pozitivnih bolnikih, ki so dva meseca uživali AGP, se je aktivacija nevtrofilcev pri inkubaciji in vitro s HP-NAP (P=0,0027) in AGP plus HP-NAP (P=0,0004) zmanjšala.
Podobne rezultate smo dobili tudi pri inkubaciji nevtrofilcev z AGP in HP-NAP (P=0,0038), ne pa s HP-NAP (P>0,05) v kontrolah.
Sharifi in Hazell (2009) sta v drugi študiji raziskala anti-H. pylori aktivnost mastike, ki je pokazala, da je večina aktivnih frakcij mastike polimer, sledita mu kislina in ista smola, medtem ko je bil nevtralni del neaktiven. Zlasti je bilo povečanje reaktivnosti opaženo tako pri oksidaciji polimera (podvojitev) kot tudi pri 4-urnem žvečenju mastife (50-odstotno povečanje).
Choli-Papadopoulou et al. (2011) so dokazali, da široka C-terminalna regija HP-NAP spodbuja adhezijo nevtrofilcev in da AGP iz CMG motijo proces vezave nevtrofilcev na endotelne celice, ki ga povzroča HP-NAP, kar je treba dodatno raziskati in bi se lahko izkoristilo v prihodnjem protivnetnem zdravljenju bolnikov s H. pylori. HP-NAP je eden od številnih dejavnikov virulence, ki jih proizvaja bakterija H. pylori. Prosti radikali, ki jih proizvajajo nevtrofilci, so ključna sestavina prirojenega imunskega sistema in učinkovito protimikrobno sredstvo proti H. pylori ter dejavnik, ki utrjuje poškodbe sluznice in gastritis. Morebitno blokiranje nastajanja reaktivnih vrst lahko privede do izboljšanja kroničnega gastritisa, povzročenega s H. pylori, in zmanjšanja znakov vnetja.
V nedavni študiji (Miyamoto et al., 2014) so preverili, katera sestavina mastike je odgovorna za delovanje proti H. pylori. Z analizo GC-MS eteričnega olja mastike so identificirali 20 sestavin, med katerimi je bilo največ α-pinena (82,26 %). Nato so avtorji preverili, katera sestavina zavira rast H. pylori. Pri desetih komercialno dostopnih spojinah so testirali antibakterijsko delovanje na seve H. pylori, ki so jih določili pri bolnikih z gastritisom, želodčno razjedo in želodčnim rakom. Nekatere od njih so pokazale antibakterijsko delovanje proti sevom, odpornim na klaritromicin in/ali metronidazol. α-terpineol in (E)-metil izoeugenol sta pokazala anti H-pylori
ne le proti sevom, občutljivim na zdravila (#09-292 iz želodčnega raka), temveč tudi proti sevom, odpornim na zdravila (#09-87 iz atrofičnega gastritisa, #09-224 iz želodčne razjede, #09-243 iz atrofičnega gastritisa). Teh 10 spojin je pokazalo tudi antibakterijsko delovanje proti trem različnim sevom (Escherichia coli, Staphylococcus aureus, Bacillus subtilis). Avtorji so zaključili, da bi bile te sestavine lahko uporabne za premagovanje rasti H. pylori v želodcu, ki je odporen na zdravila.
Ustna nega
Mastik je bil že v antiki tradicionalno zdravilo za ustni zadah in ustno higieno, to znanje pa je bilo ovrednoteno v novejših študijah. Mastik je pokazal selektivno antibakterijsko delovanje proti ustnim bakterijam Porphyromonas gingivalis (Sakagami et al., 2009; Sterer, 2006) in Prevotella melaninogenica (Sakagami et al., 2009). Študije in vivo
Protivnetne lastnosti
Kim in Neophytou (2009) sta preučevala protivnetne lastnosti mastike, ki pomagajo zmanjšati črevesno vnetje pri bolnikih z vnetno črevesno boleznijo. Za preverjanje protivnetnih lastnosti mastihe in vivo sta uporabila model kolitisa z natrijevim dekstran-sulfatom (DSS). Izvedena sta bila dva poskusa. V prvem poskusu so živali 14 dni hranili s prehrano, ki je vsebovala kombinacijo mastične smole (0,2 %) in eteričnega olja mastične smole (0,02 %); 5 dni so jih zdravili s 3-odstotnim DSS, nato pa z običajno pitno vodo. Po 14 dneh posebne prehrane so pri miših povzročili eksperimentalni kolitis z zdravljenjem s 3 % DSS v pitni vodi za 7-10 dni, medtem ko so še vedno prejemale mastično ali drugo zdravljenje. V drugem poskusu so živali hranili z različnimi dietami, kot sledi: Skupina 1 (kontrola) je prejemala običajno prehrano, skupina 2 je prejemala prehrano z 0,02 % mastičnega olja, skupina 3 je prejemala prehrano z 0,30 % γ-tokoferola, skupina 4 je prejemala prehrano z 0,02 % mastičnega olja in 0,30 % γ-tokoferola.
Podatki o živalih so pokazali, da je dodajanje mastičnega olja upočasnilo pojav in napredovanje bolezni ter pomagalo preprečiti izgubo telesne teže zaradi bolezni. Ugotovljeno je bilo, da mastično olje zagotavlja določeno zaščito pred akutnim kolitisom. Uporaba mastičnega olja v kombinaciji z γ-tokoferolom je dala podobne rezultate kot uporaba mastičnega olja ali samo γ-tokoferola.
Rezultati nedavne študije na podganah Wistar s kolitisom so pokazali protivnetne in antioksidativne lastnosti mastike. Avtorji so zaključili, da bi lahko imela mastika terapevtsko vlogo pri Crohnovi bolezni, saj uravnava oksidativno/antioksidativno ravnovesje in modulira vnetje (Gioxari et al., 2011).
V študiji Papaloisa in drugih (2012) so podganam, zdravljenim s trinitrobenzen sulfonsko kislino, posamično dajali mastiko v prahu (100 mg/kg telesne teže) ali sestavine mastike (tj. inulin, kisle frakcije AF, faktor nevtralne nekroze NF ali glavno triterpensko kislino oleanolno kislino OA). Poškodbe debelega črevesa so bile ocenjene mikroskopsko, izmerjene pa so bile tudi ravni tumorskega nekroznega faktorja α (TNF-a), interlevkina IL-6, IL-8 in medcelične adhezijske molekule 1. Vzpostavljen je bil model vnetja v kokulturah človeških epitelijskih celic debelega črevesa HT29 in monocitov/makrofagov. Izmerjeni so bili sproščanje laktatne dehidrogenaze ter ravni TNF- α, IL-8 in jedrnega faktorja-κB (NF-κB) p65. In vivo so z mastičnim prahom dosegli histološko izboljšanje kolitisa in znatno uravnavanje vnetja, tudi na ravni mRNA. Čeprav histološkega izboljšanja ni bilo opaziti, sta AF in NF zmanjšala raven vnetnih označevalcev. Inulin je bil neučinkovit. In vitro je zdravljenje z mastiko v prahu zmanjšalo IL-8 in NF-κB p65. Niti frakcije niti OA niso bile izključno bioaktivna sestavina. Avtorji so zaključili, da najverjetneje celoten mastični prah in ne njegove posamezne frakcije zmanjšujejo vnetje prek regulacije NF-κB.
Anti-ulcerozna in antioksidativna aktivnost
Leta 1986 so Al-Said in drugi izvedli študijo in vivo na morskih prašičkih, da bi ocenili učinkovitost mastihe proti razjedam želodca in dvanajstnika. V ta namen so z uporabo ustreznih kemikalij v želodcu ustvarili razjedo (aspirin, cisteamin hidroklorid itd.). Nato so jim s hrano dajali mastiko v odmerku 500 mg na kg. Rezultati študije so pokazali, da je dajanje mastike povzročilo pomembno zmanjšanje širjenja in intenzivnosti nastale razjede v želodcu morskih prašičkov, kar kaže na to, da se lahko uporablja kot zdravilo za lokalno nastalo razjedo.
Heo in drugi so leta 2006 in vivo preučevali učinek mastike na zmanjšanje poškodb, ki jih povzroča diklofenak v črevesju, in prenosa bakterij pri podganah, kar je pojav, ki ga na splošno povzročajo nesteroidna protivnetna zdravila (NSAID). V ta namen so podgane razdelili v štiri skupine; kontrolno skupino, skupino z diklofenakom, skupino z diklofenakom z 0,3 ml/kg mastife in skupino z diklofenakom z 1,0 ml/kg mastife. Mastikova olja (dodatne informacije niso bile podane) so dajali 3 ure pred dajanjem diklofenaka (100 mg/kg peroralno 2 dni). Merjeni parametri so bili črevesna prepustnost, število enteralnih aerobnih bakterij v distalnem ileumu in cekumu, črevesna adhezija, lipidna peroksidacija distalnega ileuma ter prenos bakterij v mezenterične bezgavke, jetra, vranico, ledvice oziroma srce. Ugotovljeno je bilo, da so se vsi parametri, ki so se z dajanjem diklofenaka povečali, po dajanju mastike v odmerku 1 ml/kg teže zmanjšali.
| Preizkušen zeliščni pripravek | Moč Odmerek Način dajanja | Eksperimentalni model | Referenca | Glavne neklinične ugotovitve |
| Mastika in njegovo eterično olje | Večodstotni odmerki mastikovega olja Mastik | In vitro Antibakterijsko delovanje proti Clostridium botulinum | Daifas et al., 2004 | Za inhibicijo proteolitičnih sevov Clostridium botulinum je potrebnih 0,3 % mastičnega olja |
| Mastika (skupna, kisla in nevtralna frakcija) in 3 eterična olja iz mastike, listov in vejic P. lentiscus var. chia | Ni določeno | In vitro Delovanje proti Staphylococcus aureus, Staphylococcus epidermidis, Pseudomonas aeruginosa, Entecobacter cloacae, Klebsiella pneumonia, Escherichia coli, Candida albicans, Candida tropicalis, Torulopsis glabrata | Magiatis et al., 1999 | In vitro antibakterijska/fungistatična aktivnost treh eteričnih olj in mastihe proti šestim bakterijam in trem glivam kaže, da je olje mastihe iz smole najbolj aktivno proti bakterijam in glivam, medtem ko mastiha deluje le proti bakterijam. |
| Mastika, mastikovo olje in njegove sestavine | 20 µl na papirnati disk s premerom 6 mm na 20 ml agarskega Petrijevega diska | In vitro Antibakterijsko delovanje protiS. aureus, S. epidermidis, B. subtilis in E. Coli | Koutsoudaki et al., 2005 | Mastikovo olje iz smole je najbolj aktivno proti trem testiranim sevom. Antibakterijsko delovanje je mogoče pripisati kombinaciji več sestavin in ne eni posebni spojini. Sestavine mastike, ki jih je mogoče ekstrahirati z etanolom, nimajo učinka na S. aureus, B. subtilis in E. Coli |
| Mastika v prahu | Ni določeno | In vitro Delovanje proti sevu H. pylori NCTC 11637 in šestim kliničnim izolatom bolnikov | Huwez et al., 1998 | MBC mastike, potreben za uničenje H. pylori, je bil 60 μg/ml |
| Mastika | 2000 do 1,9 µg/ml | In vitro Delovanje na 12 izoliranih kliničnih sevov H. pylori | Marone et al., 2001 | Baktericidno delovanje; EC50, 50 % sevov je bilo uničenih pri koncentraciji 125 μg/ml in 90 % pri koncentraciji 500 μg/ml |
| Vodni ekstrakti mastike | Vodni ekstrakti mastike, ki vsebujejo arabino-galaktanske beljakovine (brez nadaljnje specifikacije) | In vitro Delovanje na 12 izoliranih kliničnih sevov H. pylori | Bona et al., 2001 | Izvlečki vsaj 1,4 g mastihe vplivajo na sposobnost preživetja bakterij in preprečujejo rast celic. |
| Celotni izvleček mastike brez polimera (TMEWP) | Celotni ekstrakt mastike brez polimera (TMEWP) (brez nadaljnje specifikacije) ter njegova kisla in nevtralna frakcija | In vitro Delovanje proti 10 kliničnim izolatom H. pylori in referenčnemu sevu CCUG 38771, testirano v obdobju treh mesecev | Paraschos et al., 2007 | Izvlečki mastičnega lesa so pokazali baktericidne aktivnosti, odvisne od koncentracije in seva Najvišjo aktivnost je pokazala kisla frakcija s povprečno MBC 0,136 mg/ml, sledita TMEWP (MBC, 0,256 mg/ml) in nevtralna frakcija TMEWP (0,638 mg/ml) |
| Mastika | Peroralno, 1 g dnevno 1 mesec 2-delna študija | In vitro in in vivo 1. del: in vitro učinek AGP na aktivacijo nevtrofilcev z metodo in inkubacijo AGP s HP-NAP in nevtrofilci pri petih H. pylori pozitivnih bolnikih (3 ženske, starost 21-74 let) in treh H. pylori negativnih zdravih moških prostovoljcih (starost 23-72 let). Del 2: učinek uživanja mastičnega gumija in vivo na aktivacijo nevtrofilcev pri vseh udeležencih je naveden v preglednici 4 (Klinične študije). | Kottakis et al., 2009 | Specifična vezava arabino-galaktanskih beljakovin (AGP) na dve membranski beljakovini nevtrofilcev, kar lahko povzroči inhibicijo nevtrofilcev aktivacija Aktivacija nevtrofilcev se je zmanjšala pri inkubaciji in vitro s HP-NAP (P=0,0027) in AGP plus HP-NAP (P=0,0004) pri H. pylori pozitivnih bolnikih, ki so dva meseca uživali AGP. Podobne rezultate smo dobili tudi pri inkubaciji nevtrofilcev z AGP in HP-NAP (P=0,0038), ne pa s HP-NAP (P>0,05) pri kontrolnih skupinah |
| Mastika | Ni določeno | In vitro Delovanje proti H. pylori | Sharifi in Hazell 2009 | Najbolj aktivna frakcija mastike je bil polimer, sledita mu kislina in celotna smola, medtem ko je bil nevtralni del neaktiven. |
| Mastika | Ni določeno | In vitro | Triantafyllou et al., 2011 | Mastik je zaviral aktivnost očiščene PKC (proteinske kinaze C), zmanjšal aktivnost PKC v celičnem homogenatu in oslabil proizvodnjo superoksida v celicah, stimuliranih z aktivatorjem PKC PMA (fosforbol 12-miristat 13-acetat), in od PKC odvisnim angiotenzinom II v endotelijskih celicah. |
| Mastika | Ni določeno | In vitro Delovanje proti Porphyromonas gingivalis in Prevotella melaninogenica | Sakagami in drugi, 2009, Sterer 2006 | Mastika je selektivno antibakterijsko deloval na bakterije v ustni votlini Porphyromonas gingivalis in Prevotella melaninogenica |
| Mastikova olja (brez dodatnih informacij) | peroralno dajanje mastičnih olj 3 ure pred dajanjem diklofenaka (100 mg/kg peroralno 2 dni)
|
In vivo Pri podganah | Heo et al., 2006 | Mastikovo olje v odmerku 1 ml/kg teže je preprečilo poškodbe črevesja in bakterijsko translokacijo, ki jo je povzročil diklofenak |
| Eterično olje mastike in mastikove smole | Poskus 1) na podganah: prehrana, ki je vsebovala mastiko (0,2 %) in mastikino olje (0,02 %) 14 dni; prehrana, ki je vsebovala 3% DSS 5 dni. Po 14 dneh je bil pri miših sprožen eksperimentalni kolitis s 3-odstotnim DSS za 7-10 dni, medtem ko so še vedno prejemale mastiko ali drugo zdravljenje. Poskus 2) na miših: Skupina 1 (kontrola) običajna prehrana Skupina 2: prehrana, ki vsebuje 0,02 % mastično olje Skupina 3: prehrana z 0,30 % γ -tokoferol Skupina 4: prehrana z 0,02 % mastikovega olja in 0,30 % γ-tokoferola | In vivo Model kolitisa z natrijevim dekstran-sulfatom (DSS)Poskus 1) pri podganah Poskus 2) pri miših | Kim in Neophytou 2009 | Dopolnjevanje z mastikovim oljem je upočasnilo začetek in napredovanje bolezni ter pomagalo preprečiti izgubo telesne teže zaradi bolezni. Ugotovljeno je bilo, da mastično olje zagotavlja določeno zaščito pred akutnim kolitisom. Uporaba mastičnega olja v kombinaciji z γ-tokoferolom je dala podobne rezultate kot uporaba mastičnega olja ali samega γ-tokoferola. |
| Mastika | Peroralna uporaba 500 mg/kg | In vivo Pri morskih prašičkih z uporabo ustreznih kemikalij razjeda v želodcu | Al-Said et al., (1986) | CMG je pomembno zmanjšal širjenje in intenzivnost nastale razjede v želodčni membrani morskih prašičkov |
Sekundarna farmakodinamika
Citotoksično delovanje Citotoksično delovanje mastike in njenih glavnih spojin sta pregledala Giaginis & Theoharis (2011) v študijah in vitro, ki so dokazale, da je CMG (mastik iz Chiosa) zaviral proliferacijo rakavih celic, pridobljenih iz več vrst človeških neoplazij, med katerimi so predvsem karcinom prostate, debelega črevesa, pljuč, trebušne slinavke in hematološki malignomi. Zaščita pred aterosklerozo Raziskali so tudi možnost antiaterogenih učinkov mastike. Preučevali so biološko delovanje sline, ki izvira iz žvečenja naravne mastife, pa tudi iz žvečenja komercialnih gum (s sintetičnimi parfumi in umetnim antioksidantom ΒΗΤ), v suspenziji postopka oksidacije lipoproteina nizke gostote. Dokazana je bila biološka aktivnost sline iz petih različnih žvečilnih gumijev na zaviranje oksidacije lipoproteina nizke gostote (LDL), ki so jo in vitro povzročili bakrovi ioni, in kvantitativno izražena kot % zaščite (% Pr) (Andrikopoulos et al., 2002). Ugotovljeno je bilo, da je najbolj učinkovit surovi CMG (74,6 % Pr), ki mu je sledil komercialni CMG (64,3 % Pr). Biološko aktivne snovi v izvlečkih CMG (3 g) in v ustrezni slini (1 ura žvečenja) so bile opredeljene kot (poli)fenolne spojine v količini 0,3 oziroma 0,2 mg. Njeno zaščitno delovanje je bilo nekoliko večje celo od ustreznega delovanja vitamina Ε, ki je bil uporabljen kot osnova za primerjavo. Andrikopoulos in drugi (2003) so prav tako dokazali, da imajo triterpeni, prisotni v mastiki, izjemen antioksidativni učinek na lipoproteine nizke gostote (LDL). Na podlagi rezultatov testov so ugotovili, da je bil CMG (smola iz P. lentiscus var. Chia) najučinkovitejši naravni proizvod od vseh, ki so jih preučili (smola P. terebinthus, smola dammar, akacijev gumi, tragakantov gumi, gumi storax) pri zaščiti pred oksidacijo človeškega LDL. Najmanjši in največji odmerek za pojav nasičenja pri zaviranju oksidacije LDL sta bila 2,5 mg in 50 mg CMG (75,3 % oziroma 99,9 %). Dedoussis in drugi (2004) so preučevali učinek polarnega izvlečka smole (metanol/voda 60:40 V/V) na preživetje mononuklearnih celic periferne krvi (PBMC) v pogojih oksidativnega stresa, ki ga povzroča oksidirani lipoprotein nizke gostote (oxLDL). Med eksperimentalno študijo je izpostavljenost celic oksidirani obliki LDL povzročila hitro apoptozo in nekrozo omenjenih celic. Raziskani so bili tudi molekularni mehanizmi, s katerimi celotni polarni izvleček smole zavira citotoksični učinek oksLDL na PBMC. Pri hkratnem gojenju celic z oksLDL in polarnim izvlečkom je bilo opaženo zaviranje obeh pojavov. Antioksidativno delovanje Mastiko so različni ljudje uporabljali kot konzervans za maščobe in olja. Takšna uporaba pri egiptovskih vaščanih je v 70. letih prejšnjega stoletja sprožila prvo študijo o antioksidativni aktivnosti mastihe, v kateri sta Abdel Rahman in Youssef Soad (1975) pokazala, da ima mastika podobno antioksidativno aktivnost kot butilirani hidroksianizol. Poleg tega so bili ocenjeni molekularni mehanizmi protivnetnega delovanja in potencialna vloga antioksidativnega delovanja CMG (Triantafyllou et al., 2011), kjer je bilo ugotovljeno, da CMG zavira aktivnost prečiščene PKC (Inhibition of protein kinase C), zmanjša aktivnost PKC v celičnem homogenatu in omili proizvodnjo superoksida v celicah, spodbujenih z aktivatorjem PKC PMA (fosforbol 12-miristat 13-acetat) in PKC-odvisnim angiotenzinom II v endotelijskih celicah.Varnost farmakologija
Podatki niso na voljo.Farmakodinamične interakcije
Indukcija encimov CYP Katsanou in drugi (2014) so ugotavljali, ali mastik modulira izražanje CYP1A1 in CYP1A2 mRNA (merjeno z verižno reakcijo polimeraze z reverznim prepisom v realnem času) in aktivnost CYP1a vezane etoksiresorufin O-detilaze (EROD) v jetrih podgan po peroralni uporabi izvlečka CMG 1428 in 2000 mg/kg telesne teže. Za oceno potencialne modulacije CYP1A1/2 v jetrih podgan za oceno tveganja za ljudi smo preučevali dobro znano bioaktivno naravno spojino, kofein, za ugotavljanje potencialnih primerjalnih učinkov na jetrne encime. Dajanje izvlečka CMG v uporabljenih odmerkih ne povzroči pomembne transkripcijske modulacije CYP1A1/2 in posledične aktivnosti encima CYP1A, medtem ko dajanje kofeina v visokem odmerku 100 mg/kg telesne teže povzroči izražanje mRNA in aktivnost encima. Avtorji predvidevajo, da dajanje izvlečka CMG v odmerkih, ki presegajo priporočene farmacevtske odmerke, ne modulira presnovne aktivacije več prokancerogenih snovi, ki jo katalizira CYP1A, zato naj ne bi bilo biološko ali toksikološko pomembno v primerjavi z ustreznimi učinki, opaženimi po zdravljenju s kofeinom.Sklepi
V zadnjih 30 letih je bilo objavljenih več študij in vitro in in vivo za mastiko v prahu, pa tudi za pridobljene pripravke, frakcije in sestavine (Huwez et al., 1998; Magiatis et al., 1999; Daifas et al., 2004; Koutsoudaki et al., 2005; Bona et al., 2001; Marone et al., 2001; Paraschos et al., 2007). Podpirajo verodostojnost uporabe mastike, ki je edini rastlinski pripravek, predlagan v monografiji. Nekateri podatki so pokazali protimikrobne (predvsem proti H. pylori) ter antioksidativne in protivnetne lastnosti.Pregled razpoložljivih farmakokinetičnih podatkov o rastlinski(-ih) snovi(-ah), rastlinskem(-ih) pripravku(-ih) in ustreznih sestavinah
Čeprav se smola P. lentiscus L. (z otoka Chios) uporablja na področju prehrane, je peroralna absorpcija njenih glavnih sestavin še vedno nejasna. V okviru ugotavljanja lastnosti CMG, ki bi jih lahko pripisali terapevtskim učinkom ali učinkom prehranske vrednosti, je bila razvita in uporabljena metodologija, ki temelji na tekočinski kromatografiji visoke ločljivosti (HPLC) v povezavi s tandemsko masno spektrometrijo (MS/MS), za količinsko opredelitev triterpenskih kislin mastike, 24Z-izomastikadienonske kisline (IMNA) in 24Z-izomastikadienolske kisline (IMLA) v mišji plazmi (Lemonakis et al., 2011). Določene spojine so bile izbrane na podlagi njihove biološke aktivnosti in potenciala proti H. pylori. Koncentracije so bile hkrati določene v mišji plazmi po peroralnem vnosu mastihe ali celotnega izvlečka mastihe brez polimera (TMEWP), da bi ocenili vlogo naravnega polimera, poli-β-mircena, v procesu absorpcije. Po dajanju TMEWP pri miših so bile ravni IMNA in IMLA v plazmi znatno višje (približno 10-krat) v primerjavi z ravnmi IMNA in IMLA v plazmi po dajanju celotnega CMG, kar kaže na to, da ima polimer ključno vlogo v procesu absorpcije. Natančneje, po dajanju TMEWP so bile vrednosti Cmax v plazmi 3300±859 ng/ml za IMNA in 163±58 ng/ml za IMLA. Za primerjavo, po dajanju CMG so bile vrednosti Cmax v plazmi 329±57 ng/ml za IMNA in 28±8 ng/ml za IMLA.Pregled razpoložljivih toksikoloških podatkov v zvezi z rastlinsko(-imi) snovjo(-ami)/zeliščnim(-i) pripravkom(-i) in njegovimi sestavinami
Toksičnost enega odmerka
Podatki niso na voljo.Ponavljajoči se odmerki toksičnost
Toksičnost mastihe v prehrani so preučevali pri samcih in samicah podgan F344 (Kang et al., 2007), ki so jih 13 tednov hranili z 0 %, 0,22 %, 0,67 % in 2 %, primešanih v osnovno prehrano v prahu. V celotnem poskusnem obdobju pri nobeni živali niso opazili smrtnosti ali očitnih kliničnih znakov. Telesna teža se je v skupini, ki je bila zdravljena z visokim odmerkom, zmanjšala od 2. do konca tedna pri samcih ter v 8. in 13. tednu pri samicah. Absolutna in relativna teža jeter se je povečala v odvisnosti od odmerka ali omejeno na samce ali samice skupine z visokim odmerkom, skupaj s spremembami hematoloških parametrov, vključno s povečanjem WBC (belih krvnih celic) in trombocitov pri samcih z visokim odmerkom. Spremenjeni biokemijski parametri seruma so vključevali povečanje skupnih beljakovin, albumina in skupnega holesterola pri obeh spolih ter γ-GTP samo pri ženskah. Vendar makroskopski pregled ob nekropsii ni pokazal nobenih grobih sprememb, prav tako mikroskopski pregled ni pokazal z zdravljenjem povezanih ugotovitev v nobenem od pregledanih organov. Ker je prehransko zdravljenje z mastiko 13 tednov v tej študiji povzročilo zmanjšanje telesne mase pri visokem odmerku, zlasti pri samcih, in povečanje mase jeter v odvisnosti od odmerka pri obeh spolih brez kakršnih koli morfoloških ugotovitev, se sklene, da je pri 0,67 % v prehrani raven brez opaženih škodljivih učinkov (NOAEL).Genotoksičnost
Za mastiko ni na voljo podatkov. Vodni izvleček, imenovan Chios mastic water (CMW), ki se pogosto uporablja v izdelkih za ustno higieno, smo preučevali zaradi njegove potencialne genotoksične aktivnosti in njegovih antigenotoksičnih lastnosti proti mutageni snovi mitomicinu-C (MMC). Genotoksičnost je bila ocenjena z uporabo testa in vitro Cytokinesis Block Micro-Nucleus (CBMN) in testa in vivo Somatic Mutation and Recombination Test (SMART). Pri prvem preskusu so limfocite obdelali z 1, 2 in 5 % (V/V) CMW z ali brez MMC v koncentracijah 0,05 in 0,50 μg/ml. Pri CMW ni bilo opaziti bistvene indukcije mikronukleusov, medtem ko je sočasno zdravljenje z MMC povzročilo zmanjšanje mikronukleusov, povzročenih z MMC, ki je bilo med 22,8 % in 44,7 % (Vlastos et al., 2013). Mastikova voda je voda, ki se v velikih količinah pridobiva skupaj z mastikovim oljem med parno destilacijo mastikove smole in vsebuje vse v vodi topne sestavine mastike ter majhno količino (0,5-1 % V/V) mastikovega olja.Rakotvornost
Podatki niso na voljo.Strupenost za razmnoževanje in razvoj
Podatki niso na voljo.Lokalna toleranca
Podatki niso na voljo.Druge posebne študije
Podatki niso na voljo.Sklepi
V trimesečni študiji ponovnih odmerkov na podganah je bila edina pomembna ugotovitev zmanjšana telesna teža v skupini z visokimi odmerki. Zato je bila vrednost NOAEL 0,67 % mastike v prehrani. Drugi podatki o toksičnosti niso na voljo. Pri ocenjevanju genotoksičnosti in vitro so bili mikronukleusni testi in testi SMART opravljeni le z mastično vodo, ne pa tudi z mastičo. Vnos na seznam za mastiko ni predlagan.Splošne ugotovitve o nekliničnih podatkih
Študije in vitro so pokazale določeno protimikrobno aktivnost pripravkov iz mastike (predvsem eteričnega olja) proti grampozitivnim in delno gramnegativnim bakterijam ter zlasti aktivnost proti H. pylori, pri čemer je bila najučinkovitejša najmanjša bakterijska koncentracija (MBC) 60 μg/ml. Te ugotovitve skupaj z rezultati antioksidativnega in protivnetnega delovanja in vitro dajejo pozitiven signal za predlagano terapevtsko indikacijo mastike pri blagih dispeptičnih motnjah. Poleg tega rezultati eksperimentalnih modelov in vivo dajejo ustrezno verodostojnost dolgoletni tradicionalni medicinski uporabi mastike v predlagani terapevtski indikaciji. V eni sami študiji je bila raziskana farmakokinetika dveh najpogostejših sestavin mastike, triterpenskih kislin, 24Z-izomastikadienonske kisline (IMNA) in 24Z-izomastikadienolne kisline (IMLA), medtem ko drugi podatki o farmakokinetiki in interakcijah niso na voljo. Mastik ni induktor CYP1A1/2 v jetrih podgan. V 13-tedenski študiji toksičnosti pri ponovnih odmerkih na podganah je 0,67-odstotna vsebnost mastihe v prehrani pokazala, da ni opaženih škodljivih učinkov (NOAEL). Ker ni podatkov o strupenosti za razmnoževanje in razvoj, uporabe med nosečnostjo in dojenjem ni mogoče priporočiti. Ustrezne študije za oceno genotoksičnosti niso na voljo. Preskusi strupenosti za razmnoževanje in rakotvornosti niso bili opravljeni. Zaradi pomanjkanja ustreznih testov genotoksičnosti se vpis na seznam EU ne priporoča.Klinični podatki
Klinična farmakologija
- Pregled farmakodinamičnih podatkov o rastlinski(-ih) snovi(-ah)/pripravku(-ih), vključno s podatki o ustreznih
- Pregled farmakokinetičnih podatkov v zvezi z rastlinsko(-imi) snovjo(-ami)/pripravkom(-i), vključno s podatki o ustreznih sestavinah
Klinične študije (študije primerov in klinična preskušanja ) Preprečevanje razjed zaradi delovanja proti Helicobacter pylori
V prvi klinični študiji (Al-Habbal et al., 1984) je sodelovalo 60 prostovoljcev (60) s simptomi in endoskopsko potrditvijo razjede dvanajstnika. Za primerjavo učinkovitosti CMG (mastike iz Chiosa) so bili prostovoljci razdeljeni v dve skupini: skupina 1 je dva tedna uživala CMG (1 g na dan), skupina 2 pa je v enakem časovnem obdobju uživala enak odmerek placeba v prahu (laktoza). Po dveh tednih je bilo osemintrideset (38) prostovoljcev endoskopsko pregledanih, da bi ugotovili napredek razjede (10 prostovoljcev iz skupine CMG in 12 prostovoljcev iz skupine s placebom se ni udeležilo kontrolne endoskopije, zato so bili izločeni iz raziskave). Rezultati so pokazali, da so se v skupini, ki je uživala CMG, simptomi ublažili v 80 % primerov, endoskopski pregled pa je potrdil, da je bila razjeda dvanajstnika ozdravljena v 70 % primerov, medtem ko so bili rezultati skupine s placebom 50 % (ublažitev simptomov) oziroma 22 % (ozdravitev razjede dvanajstnika). Avtorji so zaključili, da je bila mastika pri lajšanju in zdravljenju simptomov razjede aktivnejša od placeba, medtem ko uporaba CMG ni povzročila neželenih stranskih učinkov. Komentar ocenjevalca: Visoka stopnja opustitve (skoraj 50 %), prekratko trajanje uporabe in pomanjkanje preiskav po zdravljenju onemogočajo zanesljiv zaključek o učinkovitosti, zato so, kot navajajo tudi avtorji, potrebne nadaljnje študije za določitev vloge mastike pri zdravljenju razjede. Ista raziskovalna skupina je objavila (Huwez & Al-Habbal 1986) izsledke druge klinične študije pri bolnikih z benignimi razjedami na želodcu. V ta namen so 6 bolnikom z želodčno razjedo, diagnosticirano z gastroskopijo, štiri tedne dajali CMG v odmerku 2 g na dan (1 g pred zajtrkom in 1 g pred spanjem ponoči). V obdobju najmanj dveh mesecev pred začetkom klinične študije niso prejemali nobene druge vrste farmacevtskega zdravljenja. Za oceno delovanja mastike so bile opravljene gastroskopije ter rutinske laboratorijske kontrole krvi, urina in drugih biokemičnih parametrov, in sicer pred začetkom zdravljenja, dva tedna po njem, štiri tedne po njem in dva meseca po začetku jemanja CMG. Rezultati študije so pokazali, da je dajanje zdravila CMG pri vseh šestih bolnikih povzročilo olajšanje simptomov. Pozitiven izid je bil endoskopsko potrjen pri petih od njih. Med študijo, pa tudi dva meseca po njenem zaključku, niso ugotovili nobenega neželenega učinka ali nenavadnega rezultata v laboratorijskih analizah. Leta 2003 so Roe in drugi v Južni Koreji objavili klinično študijo o delovanju mastike proti gastritisu, ki ga povzroča H. pylori. V študiji, ki jo je izvedla Medicinska fakulteta Univerze Dan-kook v Južni Koreji, je sodelovalo oseminštirideset prostovoljcev, za katere je bilo s testom UBT (tehnika UREA BREATH TESΤ za odkrivanje H. pylori) ugotovljeno, da so okuženi s H. pylori. Udeleženci so bili razdeljeni v dve skupini: prva skupina je 90 dni uporabljala žvečilni gumi mastiko (1 mg/kos) z otoka Chios, druga pa je uporabljala placebo žvečilni gumi. Test UBT je bil pri bolnikih uporabljen pred začetkom študije ter v intervalih 30 in 90 dni po zaključku. Avtorji so zaključili, da mastika ugodno vpliva na gastritis, okužen s H. pylori. Leta 2009 so Kottakis in sod. raziskovali učinke mastike na efektorje prirojenega celičnega imunskega sistema. Učinek in vivo arabinogalaktanskih beljakovin, izoliranih iz mastihe (AGP), ob prisotnosti HP-NAP (Helicobacter pylori neutrophil activating protein) pri aktivaciji nevtrofilcev so preučevali pri petih bolnikih, okuženih s H. pylori, in treh zdravih prostovoljcih, ki so dva meseca dnevno uživali 1 g CMG. Vsi udeleženci pred ali med preskušanjem niso prejemali nobenih imunosupresivnih zdravil; bolniki z infekcijskimi boleznimi, ki bi lahko spremenile njihovo imunološko stanje, so bili izključeni. Izvedene so bile tudi študije in vitro s poskusi pull-down za oceno učinka AGP ob prisotnosti HP-NAP na aktivacijo nevtrofilcev. Aktivacijo nevtrofilcev so ocenili z nikotinamid adenin dinukleotid fosfat-oksidaznimi testi in metodami optične mikroskopije z merjenjem redukcije citokroma C. Ugotovljeno je bilo, da se je aktivacija nevtrofilcev pri H. pylori pozitivnih bolnikih, ki so 2 meseca uživali AGP, zmanjšala, ko so nevtrofilce in vitro inkubirali s HP-NAP (P=0,0027) in AGP plus HP-NAP (P=0,0004). Podobne rezultate smo dobili tudi pri inkubaciji nevtrofilcev z AGP in HP-NAP (P=0,0038), ne pa s HP-NAP (P>0,05) v kontrolah. Študije kažejo, da AGP zavirajo aktivacijo nevtrofilcev v prisotnosti HP-NAP, kar ima ključno vlogo pri patologijah, povezanih s H. pylori v želodčni sluznici. V drugem kliničnem preskušanju je bil ocenjen učinek mastike na H. pylori in vivo (Dabos et al., 2010ii). V kliničnem preskušanju je sodelovalo dvainpetdeset bolnikov. Naključno so prejemali 350 mg čiste mastike trikrat na dan (tid) 14 dni (skupina A) ali 1,05 g čiste mastike (skupina B) 14 dni ali pantoprazol 20 mg dvakrat na dan (bid) in 350 mg čiste mastike tid 14 dni (skupina C) ali pantoprazol 20 mg bid in amoksicilin 1 g bid ter klaritromicin 500 mg bid 10 dni (skupina D). Prosili so jih tudi, naj vodijo dnevnik neželenih dogodkov. Eradikacijo H. pylori so testirali z UBT v povprečju 8 dni (4-14 dni) pred začetkom zdravljenja in jo ponovili v povprečju 39 dni (33-61 dni) po zaključku študijskih zdravil). Rezultati so pokazali, da ima mastik določen učinek na H. pylori in vivo. Devet bolnikov v skupinah z monoterapijo je doseglo eradikacijo, pri še desetih bolnikih pa se je vrednost UBT v primerjavi z odčitkom pred zdravljenjem zmanjšala. Eradikacija H. pylori je bila potrjena pri 4/13 bolnikov v skupini A in pri 5/13 v skupini B. Noben bolnik v skupini C ni dosegel eradikacije, pri 10/13 bolnikih v skupini D pa je bil rezultat negativen. Med skupinami A, B in C ni bilo statistično pomembnih razlik, čeprav je bil opazen trend v skupini A (p=0,08) in v skupini B (p=0,064). Razlika je bila pomembna v skupini D (p=0,01). Kombinacija mastike in pantoprazola je bila neučinkovita tako pri izkoreninjenju H. pylori kot pri bakterijski obremenitvi. Presenetljiv neuspeh kombinacije mastike in pantoprazola verjetno pojasnimo z dejstvom, da protoni zaviralcev črpalke povečajo pH želodca in s tem zmanjšajo morebitno delovanje kislih sestavin mastike, kar je verjetno posledica delovanja proti H. pylori. Ugotovljeno je bilo, da čeprav tudi monoterapija z visokim odmerkom ni dosegla sprejemljive stopnje eradikacije, se lahko uporablja kot alternativni režim pri bolnikih, ki ne želijo opraviti eradikacije z režimom trojnega zdravljenja. Vsi bolniki so mastiko dobro prenašali in o resnih neželenih dogodkih niso poročali.Olajšanje funkcionalne dispepsije
Dabos in drugi (2010i) so izvedli prvo dvojno slepo s placebom kontrolirano raziskavo, v kateri so ocenili učinke CMG pri funkcionalni dispepsiji. Oseminštirideset bolnikov (148), ki so izpolnjevali merila Rim II za funkcionalno dispepsijo, je bilo naključno razporejenih na prejemanje zdravila CMG 350 mg trikrat na dan ali placeba. Po treh tednih zdravljenja so spremembo glede na izhodiščno stanje v resnosti simptomov funkcionalne dispepsije ocenili s hongkonškim indeksom dispepsije (HKID). Na petstopenjski lestvici (0 za odsotnost, 1 za blago, 2 za zmerno, 3 za hudo in 4 za zelo hudo) je bilo ocenjenih naslednjih dvanajst simptomov dispepsije: splošna bolečina v želodcu, napihnjenost zgornjega dela trebuha, tupa bolečina v zgornjem delu trebuha, bolečina v želodcu pred obrokom, bolečina v želodcu ob tesnobi, bruhanje, slabost, bruhanje, regurgitacija kisline, zgaga, kislost v želodcu, izguba apetita. Ob koncu 3-tedenskega poskusnega obdobja je bila ocenjena tudi bolnikova splošna ocena učinkovitosti. Ocena simptomov po zdravljenju je bila v skupini CMG bistveno nižja kot v skupini s placebom ((14,78±1,78) proti (19,96±1,83)) (p<0,05). V skupini z aktivnim zdravljenjem je prišlo do pomembnega izboljšanja ((23,68±1,64) proti (14,78±1,78)) (p<0,03). V skupini s placebom ni bilo pomembnega izboljšanja ((23,27±1,73) proti 19.96±1.69)) (p=0.23). Glede na lastno globalno oceno učinkovitosti je 40 % (30/74) bolnikov v skupini s placebom pokazalo izboljšanje, medtem ko je 77 % (57/74) bolnikov v skupini z aktivnim zdravljenjem pokazalo izboljšanje simptomov (p<0,02). Posamezni simptomi, ki so se s CMG pomembno izboljšali, so bili: splošna bolečina v želodcu, bolečina v želodcu ob tesnobi, tupna bolečina v zgornjem delu trebuha in zgaga (p<0,05 za vse štiri simptome). Dokazano je bilo, da je CMG v treh tednih zdravljenja v primerjavi s placebom pomembno izboljšal zaznavanje simptomov pri bolnikih s funkcionalno dispepsijo. Pri osmih od dvanajstih simptomov ni bilo pomembnih razlik v izboljšanju simptomov. Razlike pri splošni bolečini v želodcu (1,05±0,05 proti 0,43±0,03), bolečini v želodcu ob tesnobi (0,91±0,06 proti 0,33±0,04), zgagi (0,77±0,03 proti 0,21±0,01) in tupi bolečini v zgornjem delu trebuha (0,87±0,05 proti 0,23±0,03) so bile pomembno v korist skupine, ki se je zdravila (p<0,05 za vse štiri simptome). Bolniki so CMG dobro prenašali.Crohnova bolezen
Opravljeni sta bili dve študiji (Kaliora et al., 2007i in 2007ii), da bi ocenili učinke mastike na bolnike s Crohnovo boleznijo. Študija je bila izvedena pri bolnikih z ugotovljeno blago do zmerno aktivno Crohnovo boleznijo in pri zdravih kontrolah. Deset bolnikov in osem kontrolnih oseb je bilo vključenih v štiritedensko zdravljenje z mastičnimi pokrovčki (6 pokrovčkov na dan, 0,37 g na pokrovček). V mononuklearnih celicah periferne krvi (PBMC) so pred zdravljenjem in po njem ocenili interlevkin-6 (IL-6), tumorski nekrozni faktor alfa (TNF-alfa), monocitni kemotaktični protein-1 (MCP-1), zaviralni faktor migracije makrofagov (MIF) in znotrajcelični antioksidant glutation (GSH). Zdravljenje bolnikov s CD z mastiko je zmanjšalo izločanje TNF-alfa (2,1 ± 0,9 ng/ml proti 0,5 ± 0,4 ng/ml, p=0,028). Izločanje MIF se je znatno povečalo (1,2±0,4 ng/ml proti 2,5±0,7 ng/ml, p=0,026), kar pomeni, da sta bila naključna migracija in kemotaksa monocitov/makrofagov zavrta. Pri koncentracijah IL- 6, MCP-1 in GSH ni bilo opaziti bistvenih sprememb. Ocenjevali so tudi učinke dajanja mastife na proizvodnjo citokinov v krožečih mononuklearnih celicah bolnikov z aktivno Crohnovo boleznijo (Kaliora et al., 2007ii). Avtorji so ugotovili, da mastika deluje kot imunomodulator na PBMC, saj deluje kot zaviralec TNF-alfa in spodbujevalec MIF. Čeprav so za razjasnitev vloge tega naravnega proizvoda potrebne nadaljnje dvojno slepe, s placebom nadzorovane študije na večjem številu bolnikov, je ta ugotovitev zagotovila pozitiven izid za vlogo mastike kot potencialnega regulatorja imunosti pri Crohnovi bolezni.Lastnosti lepila
Lepilne lastnosti kitov so raziskovalci ugotavljali in preučevali zadnjih trideset let (Mikhail et al., 1986, 1989; Lesesne, 1992; Yavuzer et al., 2005). Naravna smola mastike se zelo pogosto uporablja v povojih, obližih, kompresah in drugih zdravilnih sredstvih, ki se uporabljajo pri zaščiti in celjenju ran ali pooperativnih rezov. Rezultati ustreznih publikacij kažejo, da ima CMG (mastika iz Chiosa) adhezivne lastnosti, kadar se uporablja v sredstvih za prekrivanje ter sredstva za celjenje ran in rezov, hkrati pa nima neželenih stranskih učinkov na kožo (draženje, srbenje, dermatitis, depigmentacija kože itd.) kot običajne sestavine, ki se uporabljajo v zdravilnih sredstvih. Mikhail in drugi (1986; 1989) so objavili primerjavo lepilnih lastnosti treh kategorij povojev. V prvi kategoriji lepilni povoji niso vsebovali nobene dodatne sestavine, v drugi kategoriji so povoji dodatno vsebovali sestavino, ki se pogosto uporablja za take namene: tinkturo benzoina USP (aloe, tolu balzam in stirax liquid v alkoholu), v tretji kategoriji pa je bila kot ojačitveno sredstvo uporabljena mastična spojina MC (mastika 45 %, stirax liquid <5 %, metil salicilat <5 % in alkohol). Posebna študija je pokazala, da je CMG v povojih kljub uporabi benzoina izboljšal njihove lepilne lastnosti; uporaba mastike je prinesla še večje izboljšanje, kar potrjuje, da se CMG lahko uspešno uporablja pri posebni uporabi. V drugi študiji (Lesesne 1992) je bila opravljena primerjava med lepilnimi lastnostmi in nezaželenimi učinki patentiranega pripravka iz mastike (mastike 45 %, stiraksa tekočega <5 % in metil salicilata <5 %) in tinkture benzoina USP kot sestavin lepilnih povojev. Študija je bila izvedena na 300 prostovoljcih (100 moških in 200 žensk), ki so bili podvrženi plastičnim operacijam. Prostovoljci so bili razdeljeni v dve skupini: v prvi skupini so bili uporabljeni lepilni povoji s tinkturo benzoina USP, v drugi skupini pa povoji s pripravkom CMG. Prostovoljce so pooperativno pregledali po 6 dneh, 1, 3, 6 in 12 mesecih. Ocena je temeljila na elementih, kot so: pozorno preučevanje stanja rane, pojav okužb, izcedek iz rane, depigmentacija in draženje kože ter prezgodnja izguba oprijemalnih lastnosti povoja. Ugotovitve posebne študije so pripeljale do zaključka, da CMG v primerjavi s tinkturo benzoina USP nima le izjemnih adhezivnih lastnosti za sredstva za celjenje, ampak ima tudi prednost pred slednjo, saj ima izjemno manjšo možnost nastanka težav zaradi dermatitisa in draženja ali depigmentacije kože. Rezultate te študije je potrdila druga raziskovalna skupina (Yavuzer et al., 2005), ki je ugotovila, da mastika bistveno poveča lepilno delovanje samolepilnih povojev, kadar se ti uporabljajo kot edino sredstvo za prekrivanje ran in rezov.Ustna higiena
Topitsoglou-Themeli in drugi (1984; 1985) so dokazali, da lahko sistematična uporaba CMG pomembno zmanjša količino nastajajočih ali že nastalih zobnih oblog. V tej študiji je sodelovalo deset (10) prostovoljnih študentov z nizko stopnjo kariesa. Razdeljeni so bili v dve skupini: prva je deset dni žvečila CMG, druga pa placebo žvečilni gumi. Rezultati študije so potrdili, da se je v skupini, ki je uporabljala CMG, količina mikrobnih oblog močno zmanjšala. Avtorji so zaključili, da ga je mogoče učinkovito uporabljati pri preprečevanju kariesa, parodontalnih motenj in bolezni bukalne votline na splošno. V podobni klinični študiji (Takahashi et al., 2003), ki je bila objavljena leta 2003, je bilo preučeno delovanje žvečilnega gumija z naravnim CMG proti bakterijam sline in ustne votline na splošno. V ta namen je sodelovalo 20 oralno zdravih prostovoljcev, ki so bili razdeljeni v dve skupini. Prva skupina je uporabljala žvečilni gumi CMG, druga pa žvečilni gumi s placebom. V zgoščeni slini pred žvečenjem in po njem so določili in primerjali skupno število kolonij bakterij. Hkrati so pred in po 7-dnevnem sistematičnem žvečenju v obeh skupinah preučevali stopnjo gingivitisa – zobne obloge in stopnjo draženja dlesni. Rezultati so pripeljali do zaključka, da CMG vodi do prekinitve razvoja bakterij v bukalni votlini, ki so odgovorne za povzročanje obzobnih bolezni in nastanek zobnih oblog. Hkrati je CMG v primerjavi z žvečilnim gumijem s placebom povzročil bistveno nižjo stopnjo draženja dlesni, kar potrjuje, da predstavlja drastično in varno sredstvo za izboljšanje ustne higiene. Aksoy et al. (2006) so raziskovali in vitro in in vivo delovanje mastike na patogene bakterije iz družine Streptococcus mutans, ki so eden od glavnih razlogov za nastanek kariesa in bolezni ustne votline na splošno. Za laboratorijsko študijo protimikrobnega delovanja mastike (in vitro) so bili uporabljeni modelni vzorci S. mutans. Klinična študija je bila izvedena na 25 peridenčno zdravih prostovoljcih, ki so bili razdeljeni v dve skupini: prvo skupino so sestavljali tisti, ki so uporabljali mastiko, drugo pa tisti, ki so iz primerjalnih razlogov uporabljali žvečilni gumi s placebom. Učinkovitost mastihe pri omejevanju razvoja S. mutans je bila ocenjena s primerjavo vzorcev sline, ki so bili odvzeti dvema skupinama prostovoljcev pred in po 15, 45, 75, 105 in 135 minutah od trenutka, ko so začeli žvečiti mastiho in žvečilni gumi s placebom. V vsakem od omenjenih petih intervalov je bilo ugotovljeno, da je v vzorcih sline prostovoljcev iz mastične skupine prišlo do pomembnega, postopnega zmanjšanja (15 minut: 37 %, 45 minut: 48,5 %, 75 minut: 56,7 %, 105 minut: 75 minut: 56,7 %, 105 minut: 56,7 %: Po 135 minutah žvečenja je delež bakterij znašal 62,1 % celotne populacije. Nasprotno pa pri skupini žvečilnih gumijev s placebom ni bilo nobene vrste zadrževanja populacije bakterij. V zaključkih študije je ugotovljeno, da mastika predstavlja izjemno zanimivo antibakterijsko delovanje, ki ga lahko primerjamo z delovanjem antibiotikov (vankomicina) v primeru S. mutans. To delovanje mastike se zdi še posebej pomembno, saj se nanaša na omejevanje pogostih in nevarnih bakterij v ustih, S. mutans, ki so odgovorne za dekalcifikacijo zobne sklenine in tudi za številne površinske bolezni zobne proteze. Rezultati študije so pripeljali do zaključka, da pogosta uporaba mastike predstavlja pomemben dejavnik (naravni žvečilni gumi) za izboljšanje ustne higiene, vedno v kombinaciji s pogostim ščetkanjem zob.Zmanjšanje plazemskih lipidov in sladkorja v krvi
Triantafyllou et al. (2007) so preučevali učinek mastike v prahu na zmanjšanje ravni lipidov in glukoze v plazmi. Preiskovanci (n=133-93 žensk, 43 moških, starejši od 50 let) so bili naključno razporejeni v dve skupini: prva (skupina z visokim odmerkom) je dnevno zaužila 5 g mastike v prahu, druga (skupina z nizkim odmerkom) pa je dnevno prejemala raztopino mastike v prahu, ki je vsebovala eno sedmino dnevnega odmerka, ki ga je zaužila skupina z visokim odmerkom. Biokemične parametre v serumu so določali mesečno v 18-mesečnem (skupina z visokim odmerkom) in 12-mesečnem (skupina z nizkim odmerkom) obdobju spremljanja. Izvedena je bila generalizirana linearna regresija z naključnimi učinki po metodi najmanjših kvadratov. V skupini, ki je zaužila prašek CMG (skupina z visokim odmerkom), so se zmanjšali skupni holesterol, LDL, razmerje med skupnim holesterolom in HDL, lipoprotein (a), apolipoprotein A- 1, apolipoproteina B (razmerje apoB/apoA-1 se ni spremenilo), serumske glutamat oksalocetne transaminaze (SGOT), serumske glutamat-piruvat transaminaze (SGPT) in gama-glutamiltransferaze (gama- GT). Pri moških v drugi skupini (z nizkimi odmerki) so opazili znižanje ravni glukoze. Med študijo, pa tudi dva meseca po njej, ni bil ugotovljen noben nezaželen učinek, niti ni bilo nenavadnih rezultatov laboratorijskih analiz.| Vrsta študije | Zasnova študije | Preskusni izdelek(-i) | Število oseb | Vrsta predmetov | Rezultati | Statistična analiza | Klinični pomen rezultatov | |
| Razjeda želodca ali dvanajstnika in vpliv bolnikov, okuženih s H. pylori | ||||||||
| Učinkovitost pri razjedi duo- denal Al-Habbal et al. 1984 | Dvojno slepa kontrola s placebom Randomizirano 2 tedna | Skupina 1: 1 g mastike per os na dan dva tedna Skupina 2: enako odmerjanje in trajanje placeba (laktoza) | 60 prostovoljcev, starih 62-22 let naključno razdeljeni v dve skupini (zdravljenje in placebo) 38 preiskovancev na koncu, velik osip (10 CMG in 12 placebo) | Bolniki s simptomatsko in endoskopsko dokazano benigno razjedo dvanajstnika, ki v zadnjem mesecu niso jemali zdravil proti razjedi. Brez bolnikov s stenozo zaradi pylorija, nosečnic ali doječih žensk. | V skupini z mastiko so se simptomi ublažili v 80 % primerov, endoskopski pregled pa je potrdil, da je bila razjeda dvanajstnika ozdravljena v 70 % primerov rezultati skupine s placebom so bili 50 % (ublažitev simptomov) oziroma 22 % (ozdravitev razjede dvanajstnika), medtem ko uporaba CMG ni povzročila neželenih stranskih učinkov | z-statistika | Visoka stopnja opustitve (skoraj 50 %), prekratko trajanje uporabe in pomanjkanje preiskav po zdravljenju onemogočajo zanesljive zaključke o učinkovitosti. | |
| Učinkovitost pri benignih želodčnihrazjeda Huwez in Al Habbal 1986 | Nenadzorovana študija4 tedne; Nadaljnje ukrepanje: 2 meseca | mastika, ki se daje per os v odmerek 2 g na dan štiri tedne (1 g pred zajtrkom in 1 g pred spanjem ponoči) štiri tedne | 6 bolnikov: 5 moških, 1 ženska, vsi stari > 20 let (ženska, stara > 70 let, ki se ni odzvala na več ciklov cimetidina) | Bolniki z želodčno razjedo, diagnosticirano z gastroskopijo, ki v zadnjih dveh mesecih niso bili zdravljeni z blokatorji H2, bizmutom, karbenoksolonom ali sukralfatom | Rezultati so pokazali, da je dajanje mastika je vsem šestim bolnikom olajšala simptome po 7 dneh zdravljenja (v povprečju), pri petih od njih je bila ozdravitev po 4 tednih celo endoskopsko potrjena (vključno s starejšo bolnico in enim bolnikom z dvojno želodčno razjedo). Med študijo, pa tudi dva meseca po njej, ni bil ugotovljen noben nezaželen učinek, niti ni bilo nenavadnih rezultatov laboratorijskih analiz. | Ni bilo izvedeno (ni statistično pomembno) | Zelo majhno število bolnikov | |
| In-vivo študija učinkovitosti na nevtro- Phil aktivno delovanje pri bolnikih, okuženih s H. pylori Kottakis et al. 2009 | Kontrolna študija 2 meseca | AGP iz 1 g CMG dnevno 2 meseca | pet (5) bolnikov, okuženih s H. pylori (3 ženske in 2 moška; starostno obdobje 21-74 let) let) in (tri H. pylori negativni zdravi moški prostovoljci | bolnikov, okuženih s H. pylori, in treh H. pylori negativni zdravi moški prostovoljci ne prejemajo imunosupresivna zdravila pred ali med preskušanjem in ne trpijo za drugimi nalezljivimi boleznimi, ki bi lahko spremenile njihov imunološki status | Zmanjšana aktivacija nevtrofilcev pri inkubaciji nevtrofilcev in vitro s HP-NAP (P=0,0027) in AGP in HP-NAP (P=0,0004, pri H. pylori pozitivnih bolnikov, ki so 2 meseca uživali AGP. Podobne rezultate smo dobili tudi pri inkubaciji nevtrofilcev z AGP in HP-NAP (p=0,0038), ne pa s HP-NAP (p>0,05) pri kontrolnih skupinah. | Mann- Whitney U test za primerjavo Nevtrofilci aktivacijo, kot je razvidno iz merjenja zmanjšanja citokroma C med izhodiščnim obdobjem in dvema mesecema po zdravljenju. Pomembnost je določena na p<0,05. | Majhno število udeležencev, zato so potrebne nadaljnje relativno obsežne študije, da bi utemeljili potencial koristi uživanja mastike pri boleznih zgornjih in spodnjih prebavil, povezanih s H. pylori | |
Učinkovitost proti
|
Prospektivno randomizirano nadzorovano preskušanje 14 dni (UBT v povprečju opravili 8 dni (4-14 dni) pred začetek zdravljenje in ponovili v povprečju 39 dni (33-61 dni) po zaključku zdravljenja s študijskim zdravilom) | Skupina A: 350 mg CMG trikrat na dan (tid) 14 dni Skupina B: 1,05 g čistega CMG za 14 dni, Skupina C: pantoprazol 20 mg dvakrat na dan (bd)+CMG 350 mg tid 14 dni Kontrolna skupina D: ali pantoprazol 20 mg peroralno + amoksicilin 1 g peroralno + klaritromicin 500 mg peroralno 10 dni | 52 bolnikov, naključno razporejenih v skupine A, B, C in D Izstopite: 1 bolnik iz skupine A je zaključil študijo, vendar se ni vrnil na kontrolno UBT čez 5 tednov. Študijo sta zaključila 2 bolnika iz skupine Cvendar se pet tednov pozneje niso vrnili na UBT. 1 bolnik iz skupine D je zaradi neželenih učinkov (driska in trebušni krči) prenehal z zdravljenjem. | Bolniki, pri katerih je bila prisotnost H. pylori potrjena s 13C sečninskim dihalnim testom (UBT) pred vključitvijo v študijo. | Eradikacija H. pylori je bila potrjena pri 4/13 bolnikov v skupini A in pri 5/13 bolnikov v skupini B. Pri nobenem bolniku v skupini C eradikacija ni bila dosežena, medtem ko je bilo 10/13 bolnikov v skupini D negativnih. UBT. Bilo je ni bilo statistično pomembnih razlik v povprečnih vrednostih UBT v skupinah A, B in C, čeprav je bil v skupini A (p=0,08) in skupini B (p=0,064) opazen trend. Na spletni strani razlika je bila pomembna v skupini D (p=0,01). | Analiza namena zdravljenja Rezultati so prikazani kot povprečje in SEM. Parni t-test za primerjavo med vrednostmi UBT pred in poposredovanje. Pomembnost je določena na p<0,05. | Samo pilotna študija (majhna velikost) | |
| Učinkovitost pri funkcionalni dispepsiji Dabos et al. (2010i) | Prospektivno randomizirano dvojno slepo klinično preskušanje s placebom 3 tedne; Nadaljnje ukrepanje: 1 mesec | Skupina zdravljenja: kapsula s 350 mg CMG trikrat na dan per os pred obroki tri tedne Skupina s placebom: kapsula z laktozo 3-krat na dan per os pred obroki 3 tedne | Sto oseminštirideset bolnikov (148), moških in ženske, stare od 18 do 75 let, naključno razvrščene v skupino, ki je prejemala zdravilo (74), ali v skupino, ki je prejemala placebo (74). Izstopite: 4 bolniki (1 v aktivnem zdravljenju in 3 v skupina s placebom)zaradi premajhne učinkovitosti. En bolnik v aktivnem zdravljenju je bil izgubljen iz nadaljnjega spremljanja. | Bolniki, ki izpolnjujejo Rimska merila II za funkcionalno dispepsijo s simptomi, prisotnimi vsaj 12 tednov v zadnjih 9 mesecih | Primarni izid: sprememba zbirne ocene HKID glede na izhodiščno vrednost. Sekundarni rezultat: splošna ocena učinkovitosti, ki jo podajo bolniki ob koncu študije. Ocena simptomov je bila v skupini s CMG bistveno nižja kot v skupini s placebom ((14,78±1,78) vs. (19.96±1.83)) (p<0.05). Simptomi so se izboljšali pri 40 % bolnikov, ki so prejemali placebo, in pri 77 % bolnikov, ki so prejemali mastiko (p<0,02). Posamezni simptomi, ki so se s CMG pomembno izboljšali, so bili: splošna bolečina v želodcu, bolečina v želodcu ob tesnobi, tupna bolečina v zgornjem delu trebuha in zgaga (<0,05 za vse štiri simptome). | Analiza namena zdravljenja Wilcoxonovi rangirani testi za primerjavo rezultatov HKID pred in po intervenciji. Fisher’snatančen test za splošno oceno bolnikovega odziva. Rezultati so prikazani kot povprečje ± standardna napaka povprečja | Dobra klinična ustreznost s statistično pomembnimi rezultati kljub relativno majhnemu vzorcu Glavne omejitve študije: HKID še ni bil potrjen v študijski populaciji. | |
| Vpliv mastihe na proizvodnjo citokinov v mononuklearnih ušesnih celicah bolnikov z aktivno Crohnovo boleznijo Kaliora et al., 2007i Kaliora et al. 2007ii | Nadzorovana študija Crohnova bolezen 4 tedne | 2-krat 3 mastične kapice na dan (0,37 g/kapico; d, skupaj 2,2 g) za 4 tedne | 10 bolnikov in 8 zdravih kontrol Brez izpadov | Bolniki z ugotovljeno blago do zmerno aktivno Crohnovo boleznijo in zdravi kontrolni bolniki | Zdravljenje bolnikov s CD z mastiko je povzročilo zmanjšanje izločanja TNF-alfa (2,1±0,9 ng/ml proti 0,5±0,4 ng/ml, p=0,028). Sproščanje MIF se je znatno povečalo (1,2 ± 0,4 ng/ml proti 2,5 ± 0,7 ng/ml, P=0,026), kar pomeni, da sta bili naključna migracija in kemotaksa monocitov/makrofagov zavrti. Pri IL-6, MCP-1 in GSH niso opazili bistvenih sprememb. koncentracije. | Rezultati so izraženi kot povprečje ± SE. Mann-Whitney Test za primerjavo razlik med bolniki in kontrolami pred posegom. Pomembnost je določena pri p<0,05 | Predhodna študija. Potrebne so nadaljnje dvojno slepe, s placebom nadzorovane študije na večjem številu bolnikov, da bi razjasnili vloga tega naravnega izdelka pri zdravljenju bolnikov s CD | |
| Učinkovitost žvečenje mastike pri zmanjševanju zobnih oblog Topi- tsoglou- Themeli et al. 1984; 1985 | Placebo nadzorovana študija 10 dni | skupina: mastiko žvečijo 10 dni Skupina s placebom: žvečenje placeba 10 dni | 10 prostovoljcev razdelimo v skupino z zdravilom in skupino s placebom. | Osebe z nizko stopnja kariesa | Zmanjšanje zobozdravstvenih oblog v skupini za zdravljenje | Ni znano | Majhna študija statistični podatki in rezultati niso podrobno opisani. | |
| Učinkovitost pri zmanjševanju lipidov v plazmi in sladkorja v krvi Trianta- fyllou et al. 2007 | Naključna kontrolna študija Obdobje spremljanja: Skupina z visokim odmerkom: 18-mesečna skupina: 18 mesecev Skupina z nizkimi odmerki: 12-mesečna | Skupina z visokim odmerkom: 5 g mastičnega prahu dnevno per os. Skupina z nizkimi odmerki: Raztopina CMG, ki vsebuje eno sedmino dnevnega odmerka, ki ga jemlje skupina z visokim odmerkom, per os dnevno. | n=133 (93 žensk, 43 moških), starejših od 50 let, naključno razporejenih v skupino z visokim odmerkom (45) in skupino z nizkim odmerkom (83) | Zdravi prostovoljci | Biokemične parametre v serumu so določali mesečno v obdobju 18 mesecev. (skupina z visokim odmerkom) in 12-mesečno obdobje spremljanja (skupina z nizkim odmerkom). Skupina z visokimi odmerki: zmanjšanje skupnega holesterola, LDL, razmerja med skupnim holesterolom in HDL, lipoproteinov (a), apolipoproteinA-1, apolipoproteina B (razmerje apoB/apoA-1 se ni spremenilo), vrednosti SGOT, SGPT in gama- GT. Skupina z nizkimi odmerki: znižanje ravni glukoze pri moških | Splošna linearna regresija z naključnimi učinki po metodi najmanjših kvadratov | Podpira varnost peroralne uporabe mastike | |
Klinične študije na posebnih populacijah (npr. starejši in otroci).
Podatki niso na voljo.
Splošne ugotovitve o klinični farmakologiji in učinkovitosti
Peroralna uporaba
V obstoječih preskušanjih (na približno 300 osebah) so ocenjevali peroralno uporabo mastike za lajšanje simptomov, povezanih z razjedo želodca ali dvanajstnika, ali za lajšanje simptomov funkcionalne dispepsije.
Ugotovljena je bila le ena dvojno slepa, s placebom kontrolirana klinična študija (Al-Habbal et al. 1984). Večina študij je majhnih in ima metodološke pomanjkljivosti, kot so: merila za vključitev niso dobro opredeljena, visoka stopnja izpadov (do 50 %), primarna končna točka ni vedno opredeljena in ni faze spremljanja. Ob upoštevanju vseh teh pomanjkljivosti imajo rezultati omejeno vrednost in se ne štejejo za zadostne za utemeljitev dobro uveljavljene uporabe zdravila v skladu s členom 10a Direktive 2001/83/ES.
Kožna uporaba
Kombinacija lepila za rane, ki vsebuje mastiko z drugimi spojinami (stiraks, metil salicilat in etanol), je bila prav tako klinično preizkušena na koži v primerjavi z lepilom za rane, ki vsebuje tinkturo benzoina USP (aloe, tolu balzam in stiraks v alkoholu). Študija je bila izvedena pri 300 bolnikih (200 žensk in 100 moških), razdeljenih v dve skupini, pri katerih so bili opravljeni plastični kirurški posegi in ki so jih spremljali vsaj 16 mesecev pοstoperativno. Avtorji so poročali o boljših rezultatih glede trdnosti lepila brez neželenih učinkov v skupini, ki je uporabljala lepilo za rane, ki je vsebovalo mastiko. Pozitivni rezultati teh preskušanj ne morejo potrditi nobene terapevtske indikacije.
Obstoječi rezultati kliničnih preskušanj ne zadostujejo za utemeljeno indikacijo za uporabo, lahko pa podpirajo predlagano peroralno uporabo pri blagih dispeptičnih motnjah.
Klinična Varnost/Farmakovigilanca
Pregled toksikoloških/varnostnih podatkov iz kliničnih preskušanj na ljudeh
Podatki niso na voljo.
Izpostavljenost pacienta
Poleg znane uporabe v ljudskem zdravilstvu in podatkov iz kliničnih preskušanj ni konkretnih podatkov o izpostavljenosti bolnikov.
Mastiko v kombiniranem izdelku so klinično testirali tudi na koži, pri čemer niso poročali o neželenih učinkih. To bi lahko potrdilo varno uporabo na koži.
Neželeni dogodki, resni neželeni dogodki in smrtni primeri
O neželenih dogodkih, resnih neželenih dogodkih in smrtnih primerih doslej niso poročali.
Le dva primera sta opisala alergijski kontaktni dermatitis zaradi medicinskih lepilnih povojev, ki vsebujejo komercialni kombinirani izdelek za tekoče lepilo z mastiko (Worsnop et al., 2007; Meikle et al., 2012).
Laboratorijske ugotovitve
Podatki niso na voljo.
Varnost pri posebnih skupinah prebivalstva in v razmerah na spletni strani
Podatki niso na voljo.
- Uporaba pri otrocih in mladostnikih
Podatki niso na voljo.
Kontraindikacije
Preobčutljivost na zdravilno učinkovino.
Posebna opozorila in previdnostni ukrepi za uporabo
Za zagotovitev varne uporabe je treba označiti naslednjo izjavo: Če se pojavijo neželeni učinki, se je treba posvetovati z zdravnikom ali usposobljenim zdravstvenim delavcem.
Medsebojno delovanje z zdravili in druge oblike interakcij
O medsebojnem delovanju zdravil iz kliničnih preskušanj ali študij primerov doslej niso poročali.
Plodnost, nosečnost in dojenje
Podatki o plodnosti niso na voljo.
Varnost med nosečnostjo in dojenjem ni bila ugotovljena. Ker ni zadostnih podatkov, uporaba med nosečnostjo in dojenjem ni priporočljiva.
Predoziranje
Podatki niso na voljo.
Vpliv na sposobnost vožnje ali upravljanja strojev ali slabše duševne sposobnosti
Podatki niso na voljo.
Varnost v drugih posebnih situacijah
Ne uporablja se.
Splošne ugotovitve o klinični varnosti
Doslej iz kliničnih preskušanj ali študij primerov niso poročali o neželenih dogodkih, resnih neželenih dogodkih ali smrtnih primerih ter o medsebojnem delovanju zdravil.
Informacije o varnosti so omejene, saj sta le dva primera opisala alergijski kontaktni dermatitis zaradi medicinskih lepilnih povojev, ki vsebujejo komercialni tekoči lepilni kombinirani izdelek z mastiko.
Splošne ugotovitve (ocena razmerja med koristjo in tveganjem )
Obstaja več kliničnih študij, ki so preučevale peroralno uporabo mastihe (samostojno) ali kožno uporabo mastihe (v kombinaciji). Večina je majhnih in metodološko pomanjkljivih, zato ne morejo potrditi nobene dobro uveljavljene indikacije za uporabo smole P. lentiscus L. (mastike). Vendar pa lahko te raziskave podpirajo tradicionalno uporabo, saj niso sprožile nobenih pomislekov glede varnosti.
Prah smole P. lentiscus L. se že več kot 30 let uporablja v tradicionalni in ljudski medicini v več državah (Irak, Iran, Turčija, ZDA itd.) in tudi v Evropski uniji (Grčija).
Na podlagi razpoložljivih podatkov iz različnih literaturnih virov se šteje, da so zahteve za tradicionalno uporabo v skladu z Direktivo 2001/83/ES izpolnjene za uporabo praškaste mastike v medicini.
Mastikin prah kot rastlinska snov se je uporabljal za kožno uporabo (4-40 %), medtem ko so po podatkih poročevalca v zadnjih letih (80-ih) vse galenske formule, ki so bile izdane v lekarnah in na zdravniški recept, vsebovale 9-11 % za uporabo pri kožnih težavah, kot so manjša vnetja.
Rezultati nekliničnih študij in vitro kažejo na določeno protimikrobno delovanje. Mastik naj bi izkazoval posebno močno aktivnost proti H. pylori.
Študije o toksičnosti so redke, vendar iz študije ponovnih odmerkov na podganah (vrednost NOAEL je bila 0,67 % mastihe v prehrani) in dolgotrajne uporabe v tradicionalni medicini že več kot 30 let ne izhajajo nikakršni pomisleki glede predlaganih pogojev uporabe. V monografijo so vključene naslednje indikacije za tradicionalno uporabo:
Navedba 1)
Tradicionalno zdravilo rastlinskega izvora, ki se uporablja pri blagih dispeptičnih motnjah.
Uporaba pri otrocih in mladostnikih, mlajših od 18 let, zaradi pomanjkanja ustreznih podatkov ni bila določena.
Navedba 2)
Tradicionalno zdravilo rastlinskega izvora, ki se uporablja za simptomatsko zdravljenje manjših vnetij kože in kot pomoč pri celjenju manjših ran.
Uporaba pri otrocih, mlajših od 12 let, zaradi pomanjkanja ustreznih podatkov ni bila določena. Podatki o plodnosti niso na voljo.
Varnost med nosečnostjo in dojenjem ni bila ugotovljena. Ker ni zadostnih podatkov, uporaba med nosečnostjo in dojenjem ni priporočljiva.
Glede na rezultate različnih kliničnih študij niso poročali o neželenih učinkih in rastlinski pripravek so dobro prenašali. Le dva primera sta opisovala alergijski kontaktni dermatitis zaradi medicinskih lepilnih povojev, ki so vsebovali komercialni tekoči lepilni kombinirani izdelek z mastiko.
HMPC ne more prepoznati nobene sestavine z znano terapevtsko aktivnostjo ali aktivnim označevalcem. Vnos na seznam Evropske unije ni podprt zaradi pomanjkanja ustreznih podatkov o genotoksičnosti.




